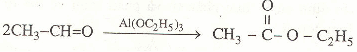Bài 1 tớ cũng ra khác đáp số ^^
Một bình kín dung tích 11,2 lít có chứa 6,40 g O2 và 1,36 g hỗn hợp khí A gồm 2 ankan. Nhiệt độ trong bình là 0oC và áp suất là p1 atm. Bật tia lửa điện trong bình kín đó thì hỗn hợp A cháy hoàn toàn. Sau phản ứng, nhiệt độ trong bình là 136,50C và áp suất là p2 atm. Nếu dẫn các chất trong bình sau phản ứng vào dung dịch Ca(OH)2 lấy dư thì có 9,00 gam kết tủa tạo thành. Biết rằng số mol ankan có phân tử khối nhỏ nhiều gấp 1,5 lần số mol của ankan có phân tử khối lớn.
1.Phần trăm thể tích của ankan có PTK nhỏ trong hỗn hợp là:
Câu trả lời của bạn:
A. 40 %
B. 30 %
C. 60 %
D. 70 %
Câu này đơn giản mà lúc đầu không để ý

)
[TEX]\frac{V_{nho}}{V_{lon}}= \frac{n_{nho}}{n_{lon}} = ,15[/TEX]
[TEX]%V_{nho} = \frac{1,5}{2,5}= 60%[/TEX]
2.Tính p1 và p2 biết rằng thể tích bình không đổi.
Câu trả lời của bạn:
A. p1 = 0,81 atm
p2 = 0,5 atm
B. p1 = 0,5 atm
p2 = 0,81 atm
C. p1 = 0,45 atm
p2 = 0,81 atm
D. p1 = 0,5 atm
p2 = 0,85 atm
[TEX]n_{CO_2} = 0,09 (mol) [/TEX]
[TEX]n_{O_2} = 0,2(mol)[/TEX]
Ta có :
[TEX]m_C + m_H = 1,36 [/TEX]. Cùng 1 khối lượng, thì H2 càng nhiều lượng O2 dùng để đốt cháy càng lớn. Lượng O2 lớn nhất để đốt [TEX][/TEX]
[TEX]n_{O_2 max} = n_C + \frac{1,36- 0,09.12}{4} = 0,16<0,2 \to O_2 du. Ankan het.[/TEX]
[TEX]n_{H} = 1,36-0,09.12 = 0,28[/TEX]
[TEX]n_C:n_H = 9:28[/TEX]
[TEX]\overline{n} : \frac{2 \overline{n}+2} = 9:28[/TEX]
[TEX]\overline{n} = 1.8 \Rightarrow CH_4[/TEX]
[TEX]C_mH_{2m+2} : a mol (m>1)[/TEX]
[TEX]\left{ \sum_C = 0,09 \\ \sum_{H} = 0,28 \right. \Rightarrow \left{ 1,5 a + a.m = 0,09 \\ 1,5a. 4 + (2m+2) a = 0,28[/TEX]
[TEX]\Leftrightarrow \left{ a=0,02 \\ m = 3[/TEX]
[TEX]\Rightarrow \left{ CH_4 : 0,03 (mol) \\ C_3H_8 : 0,02 (mol) [/TEX]
[TEX]p_1 = \frac{(0,02+0,03+0,2).0,082.273}{11,2}= 0,5(atm)[/TEX]
Số mol sau phản ứng :
[TEX]n_2 = n_{CO_2} + n_{H_2O } + n_{O_2 du} = 0,27(mol) [/TEX]
[TEX]p_2 =0,81 (atm) [/TEX]
!!!!!!!!!!
 H6 và H2 là 0,5 và 4.5mol
H6 và H2 là 0,5 và 4.5mol