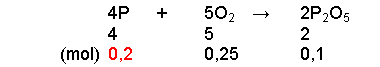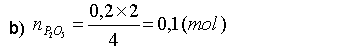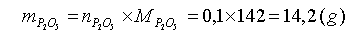H
hoangkhuongpro
bai này thì dùng bảo toàn khối lượng hoặc bảo toàn nguyên tố thì đc :Bài tập tiếp tục cho dạng này nhé:
Bài 3: Cho 112g Fe tác dụng với dung dịch axit cohidric (HCl) tạo ra 254g Sắt (II) clorua và 4g khí hidro bay lên. Khối lượng axit clohidric đã dùng là?
Bài 4: Đốt 58g khí butancần dùng 208g khí oxi và tạo ra 90g hơi ngước và khí cacbonic. Khối lượng [TEX]CO_2[/TEX] sinh ra là?
B3:146g
B4:176g