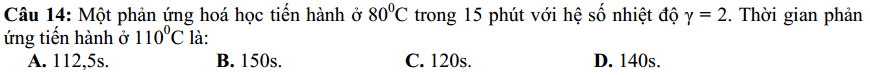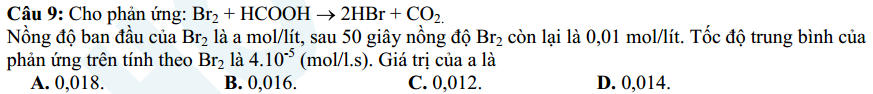W
You are using an out of date browser. It may not display this or other websites correctly.
You should upgrade or use an alternative browser.
You should upgrade or use an alternative browser.
T
tamtam96
Bạn nào thử sức với câu này không ?
Điện phân dung dịch chứa 0,1 mol $FeCl_3$, 0,2 mol $CuSO_4$ và 0,1 mol HCl ( điện cực trơ và có màng ngăn). Khi catot bắt đầu có khí bay ra thì dừng điện phân. Tại thời điểm này khối lượng dung dịch giảm bao nhiêu ???
giải:
đầu tiên Fe3+ xuống Fe2+
sau đó Cu2+ xuống Cu
và sau là sự điện phân của H+
nên tổng e cho là 0,1+0,2*2=0,5
mà n clo=0,4
còn có sự đp của nước ở anot O2=0,025 mol
lượng dd giảm = 0.2*64+0,4*35,5+0,025*32=27,8g
cho mình tham gia với
P
phamthimai146
Bạn nào thử sức với câu này không ?
Điện phân dung dịch chứa 0,1 mol $FeCl_3$, 0,2 mol $CuSO_4$ và 0,1 mol HCl ( điện cực trơ và có màng ngăn). Khi catot bắt đầu có khí bay ra thì dừng điện phân. Tại thời điểm này khối lượng dung dịch giảm bao nhiêu ???
Các phản ứng điện phân xảy ra cho đến khi catot bắt đầu có khí bay ra:
FeCl3 ----> FeCl2 + 0,5 Cl2
0,1-----------------------0,05
CuSO4 + 2 HCl ---> Cu + Cl2 + H2SO4
0,05-------0,1--------0,05--0,05
CuSO4 + H2O --> Cu + 0,5 O2 + H2SO4
0,15----------------0,15----0,075
==> FeCl2 không điện phân
khối lượng dd giảm = mCu + mCl2 + mO2 = 64*0,2 + 71*0,1 + 32*0,075 = 22,3
N
nguyenvancuong1225@gmail.com
điện phân sao không bổ sung dạng bài tập áp dụng CT Fá cả đấy
1/ Điện phân có màng ngăn 500ml dung dịch chứa hỗn hợp gồm $CuCl_2$ 0,1M và NaCl 0,5M (điện cực trơ, Hiệu suất điẹn phân là 100%) cường độ dòng điện là 5A, trong 3860s. Dung dịch thu được sau điện phân có khả năng hòa tan m gam Al. Giá trị lớn nhất của m là:
A. 2,7g
B. 5,4g
C. 4,05g
D. 1,35g
N
nguyenvancuong1225@gmail.com
Bạn nào thử sức với câu này không ?
Điện phân dung dịch chứa 0,1 mol $FeCl_3$, 0,2 mol $CuSO_4$ và 0,1 mol HCl ( điện cực trơ và có màng ngăn). Khi catot bắt đầu có khí bay ra thì dừng điện phân. Tại thời điểm này khối lượng dung dịch giảm bao nhiêu ???
Bài này đáp án là:
Bắt đầu có khí thì có:
Fe3+ -> Fe2+
Cu2+ --> Cu.
mol e = 0,1 + 0,4 = 0,5
--> mol Cl_2 = 0,2 mol
mol O2 = (0,5-0,4)/4 = 0,025 mol
$m_{giảm}$ = $m_{Cu} + m_{Cl_2} + m_{O_2}$ = 27,8 gam
T
tuonghuy333_2010
$n_{CuCl_2}=0,05(mol) \\ \\ n_{NaCl}=0,25(mol) \\ \\ Cu → Cu^{2+}+2e \\ \\ H_2O+1e → \frac{1}{2}H_2+OH^- \\ \\ → n_{NaOH}=0,1(mol) → m_{Al}=2,7(gam)$
1/ Điện phân có màng ngăn 500ml dung dịch chứa hỗn hợp gồm $CuCl_2$ 0,1M và NaCl 0,5M (điện cực trơ, Hiệu suất điẹn phân là 100%) cường độ dòng điện là 5A, trong 3860s. Dung dịch thu được sau điện phân có khả năng hòa tan m gam Al. Giá trị lớn nhất của m là:
A. 2,7g
B. 5,4g
C. 4,05g
D. 1,35g
N
nguyenvancuong1225@gmail.com
$n_{CuCl_2}=0,05(mol) \\ \\ n_{NaCl}=0,25(mol) \\ \\ Cu → Cu^{2+}+2e \\ \\ H_2O+1e → \frac{1}{2}H_2+OH^- \\ \\ → n_{NaOH}=0,1(mol) → m_{Al}=2,7(gam)$
Catot:
$Cu^{2+} +2e \rightarrow Cu$
$0,05mol \ \ \ \ \ 0,1$
$2H_2O +2e \rightarrow H_2 + 2OH^-$
$ \ \ \ \ \ \ 0,1 \ \ \ \ \ \ \ \ \ \ \ \ \ \ \ \ \ \ \ \ 0,1$
Anot:
$2Cl^- \rightarrow Cl_2 + 2e$
$ \ \ \ \ \ \ \ \ \ \ \ 0,1 \ \ \ \ \ \ 0,2$
$H_2O \rightarrow O_2 + 4H^+ + 4e$
$2Al + 2OH^- + 2H_2O \rightarrow 2AlO_2^- + 3H_2$
$0,1 \ \ \ 0,1$
--> m = 2,7 g
N
nguyenvancuong1225@gmail.com
Mấy nay mình bận quá, giờ chúng ta làm vài bài lí thuyết Hoá Học nhá các bạn:
Câu 1: Cân bằng phản ứng:
$Fe_3O_4 + KMnO_4 + KHSO_4 \rightarrow Fe_2(SO_4)_3 + MnSO_4 + K_2SO_4 + H_2O$
Câu 2: Số phát biểu đúng trong số các phát biểu sau:
_Hỗn hợp $Na_2O$ + $Al_2O_3$ tỉ lệ 1:1 tan hết trong nước dư
_Hỗn hợp tỉ lệ $Fe_2O_3$ + Cu 1:1 tan hết trong dung dịch HCl dư
_Hỗn hợp tỉ lệ $KNO_3$ + Cu 1:1 tan hết trong dung dịch $NaH_SO_4$ dư
_Hỗn hợp tỉ lệ FeS + Cú 1:1 tan hết trong dung dịch HCl dư
Còn tiếp...
Câu 1: Cân bằng phản ứng:
$Fe_3O_4 + KMnO_4 + KHSO_4 \rightarrow Fe_2(SO_4)_3 + MnSO_4 + K_2SO_4 + H_2O$
Câu 2: Số phát biểu đúng trong số các phát biểu sau:
_Hỗn hợp $Na_2O$ + $Al_2O_3$ tỉ lệ 1:1 tan hết trong nước dư
_Hỗn hợp tỉ lệ $Fe_2O_3$ + Cu 1:1 tan hết trong dung dịch HCl dư
_Hỗn hợp tỉ lệ $KNO_3$ + Cu 1:1 tan hết trong dung dịch $NaH_SO_4$ dư
_Hỗn hợp tỉ lệ FeS + Cú 1:1 tan hết trong dung dịch HCl dư
Còn tiếp...
K
kth3.ultjmate
K
kth3.ultjmate
K
kth3.ultjmate
K
kth3.ultjmate
N
nguyenvancuong1225@gmail.com
ta có $\gamma^{\dfrac{t_2-t_1}{10}}$ = $\dfrac{V_{t_2}}{V_{t_2}}$
--> $V_{t_2} = 8V_{t_1}$ --> $t_2 = \dfrac{1}{8}t_1$ --> t_2 = 1,875' = 112,5 s
N
nguyenvancuong1225@gmail.com
Ta có V = $\dfrac{C_1 - C_2}{\Delta t} = \dfrac{a-0,01}{50} = 4.10^{-5} \dfrac{mol}{l.s}$ --> a = 0,012 M
N
nguyenvancuong1225@gmail.com
ta có $\gamma^{\dfrac{40-20}{10}} = \dfrac{27}{3}$ --> $\gamma$ = 3
--> ở $55^oC$ thì phản ứng cần 34,64 s để kết thúc
N
nguyenvancuong1225@gmail.com
Chỉ còn 4 tháng nữa là các bạn 96, 95 thi Đại Học rồi, Mình xin lấy Topic này là nơi trao đổi về các câu hỏi trong các đề thi thử của các trường.
Bên cạnh đó là những câu hỏi khó của các em 11, 10 cũng được giải đáp tại đây.
:khi (176): Ôn tập Hoá Học với phương châm: Kiến thức hiện đại phương pháp Hai Lúa[Hữu]
Bên cạnh đó là những câu hỏi khó của các em 11, 10 cũng được giải đáp tại đây.
:khi (176): Ôn tập Hoá Học với phương châm: Kiến thức hiện đại phương pháp Hai Lúa[Hữu]
N
nguyenvancuong1225@gmail.com
Giải nhanh nhá các bạn:
Cho 16 gam hỗn hợp X gồm Fe, Cu, Zn ác dụng vơi oxi thu được 19,2 g chất rắn Y. Hoà tan hết Y trong dung dịch $H_2SO_4$ đặc nóng dư thấy thoát ra V lít $SO_2$( sản phẩm khử duy nhất), cô cạn dung dịch được 49,6 g chất rắn khan. Tính V.
Cho 16 gam hỗn hợp X gồm Fe, Cu, Zn ác dụng vơi oxi thu được 19,2 g chất rắn Y. Hoà tan hết Y trong dung dịch $H_2SO_4$ đặc nóng dư thấy thoát ra V lít $SO_2$( sản phẩm khử duy nhất), cô cạn dung dịch được 49,6 g chất rắn khan. Tính V.
V
vuthienthien
Giải nhanh nhá các bạn:
Cho 16 gam hỗn hợp X gồm Fe, Cu, Zn ác dụng vơi oxi thu được 19,2 g chất rắn Y. Hoà tan hết Y trong dung dịch $H_2SO_4$ đặc nóng dư thấy thoát ra V lít $SO_2$( sản phẩm khử duy nhất), cô cạn dung dịch được 49,6 g chất rắn khan. Tính V.
$nO =\frac{19,2 - 16}{16} $= 0,2 mol
$nSO4^{2-} = \frac{49,6 - 16}{96} $=0,35 mol
=>ne nhường = 0,35.2 =0,7 mol
BTe: ne nhường = 2nSO2 + 2nO => nSO2 = 0,15 mol => VSO2 = 3,36 l
N
nguyenvancuong1225@gmail.com
$nO =\frac{19,2 - 16}{16} $= 0,2 mol
$nSO4^{2-} = \frac{49,6 - 16}{96} $=0,35 mol
=>ne nhường = 0,35.2 =0,7 mol
BTe: ne nhường = 2nSO2 + 2nO => nSO2 = 0,15 mol => VSO2 = 3,36 l
Hoàn thành:
$CrO_4^{2-} + H^+ \rightarrow$
$Cr_2O_7^{2-} + OH^- \rightarrow$
Last edited by a moderator:
N
nguyenvancuong1225@gmail.com
Đốt cháy 1,92g Mg và 4,48g Fe với vừa đủ hỗn hợp X gồm khí Clo và Oxi, sau phản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua, hoà tan Y bằng một lượng vừa đủ 120ml HCl 2M, thu được dung dịch Z. Cho $AgNO_3$ dư vào Z thu được 56.69g kết tủa. Tính % Clo trong X
A. 51,72%
B. 62,5%
C. 53,85%
D. 56,36%
A. 51,72%
B. 62,5%
C. 53,85%
D. 56,36%