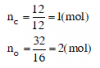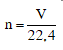CHƯƠNG 3: MOL VÀ TÍNH TOÁN HÓA HỌC
I. MOL
1.Mol là gì?
Mol là lượng chất có chứa 6.1023 nguyên tử hoặc phân tử của chất đó.
Con số 6.1023 được gọi là số Avogađro, kí hiệu là N
2.Khối lượng mol
Khối lượng mol ( kí hiệu là M) của một chất là khối lượng tính bằng gam của N nguyên tử hoặc phân tử chất đó.
Đơn vị: g/mol
Khối lượng mol có cùng số trị với nguyên tử khối hay phân tử khối của chất đó.
3.Thể tích mol của chất khí
Thể tích mol của chất khí là thể tích chiếm bởi N phân tử chất khí đó.
Trong đktc ( 0°C và 1 atm) thì thể tích 1 mol chất khí là 22,4 lít.
II. Chuyển đổi giữa khối lượng, thể tích và lượng chất
1. Chuyển đối giữa lượng chất và khối lượng chất
m = n x M (g) → n = m/M ; M = m/n
2. Chuyển đổi giữa lượng chất và thể tích khí
V = 22,4 x n (l)
 III.Tỉ khối của chất khí
III.Tỉ khối của chất khí
1. Tỉ khối của chất khí
a. Chất khí A với chất khí B
Dùng để so sánh khi A nhẹ hơn hay nặng hơn khí B bao nhiêu lần
Kí hiệu dA/B
Cách tính:

Khi dA/B > 1 ⇒ khí A nặng hơn khí B
dA/B = 1 ⇒ khí A bằng khí B
dA/B < 1 ⇒ khí A nhẹ hơn khí B
b.Chất khí A với không khí
Tương tự như phần a. không khí đóng vai trò như chất khí B với Mkk = 29(g/mol)
Kí hiệu dA/kk
2.Thí dụ
So sánh khí oxi với không khí

⇒ Oxi nặng hơn không khí 32/29 lần
IV.Tính theo công thức hóa học
1. Biết CTHH, xác định thành phần phần trăm theo khối lượng các nguyên tố trong hợp chất
Thí dụ: xác định thành phần phần trăm khối lượng các nguyên tố trong CO2
Cách làm
Tìm khối lượng mol của hợp chất: mCO2 = 12+16×2 = 44 (g/mol)
Tìm số mol nguyên tử mỗi nguyên tố trong 1 mol hợp chất:
Trong 1 mol CO2 có 1 mol C; 2 mol O
Thành phần phần trăm theo khối lượng:
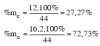 2. Biết thành phần nguyên tố, tìm CTHH
2. Biết thành phần nguyên tố, tìm CTHH
Thí dụ: một hợp chất có thành phần các nguyên tố theo khối lượng là 27,27 % C; 72,73 % O. Xác định CTHH của hợp chất biết M = 44 g/mol
Cách làm
Tìm khối lượng mỗi nguyên tố trong 1 mol hợp chất

Tìm số mol nguyên tử mỗi nguyên tố trong 1 mol hợp chất:
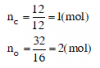
Vậy trong 1 mol hợp chất có 1 mol C; 2 mol O
CTHH: CO2
V.Tính theo phương trình hóa học
1. Tìm khối lượng chất tham gia và chất sản phẩm
Cách làm:
Bước 1: Viết phương trình
Bước 2: tính số mol các chất
Bước 3: dựa vào phương trình tính được số mol chất cần tìm
Bước 4: tính khối lượng
Thí dụ 1: cho 4g NaOH tác dụng với CuSO4 tạo ra Cu(OH)2 kết tủa và Na2SO4. Tính khối lượng Na2SO4
Các bước tiến hành
Viết PTHH và cân bằng
2NaOH + CuSO4 → Cu(OH)2↓ + Na2SO4
Tính số mol NaOH tham gia phản ứng
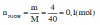
Tính số mol Na2SO4 thu được
Theo PTHH: 1 mol NaOH phản ứng thu được 0,5 mol Na2SO4
Vậy: 0,1 mol NaOH…………………0,05 mol Na2SO4
Tìm khối lương Na2SO4 thu được
mNa2SO4 = n×M = 0,05×142 = 7,1g
Thí dụ 2: Tính khối lương NaOH cần dùng để điều chế 7,1g Na2SO4
Viết PTHH:
2NaOH + CuSO4 → Cu(OH)2↓ + Na2SO4
Tính số mol Na2SO4 sinh ra sau phản ứng

Tìm số mol NaOH tham gia phản ứng
Theo PTHH: để điều chế 1 mol Na2SO4 cần dùng 2 mol NaOH
Vậy muốn điều chế 0,05 mol Na2SO4 cần dùng 0,1 mol NaOH
Tính khối lương NaOH cần dùng
mNaOH = n×M = 0,1×40 = 4(g)
2. Tìm thể tích chất khí tham gia và sản phẩm
Cách làm:
Bước 1: Viết PTHH
Bước 2: Tìm số mol khí
Bước 3: thông qua PTHH, tìm số mol chất cần tính
Bước 4: Tìm thể tích khí
Thí dụ 1: Lưu huỳnh cháy trong oxi hoặc trong không khí sinh ra lưu huỳnh đioxit SO2. Hãy tính thể tích (đktc) sinh ra, nếu có 4g khí O2 tham gia phản ứng
Viết PTHH
S + O2 → SO2 (t0)
Tìm số mol O2 sinh ra sau phản ứng:
Tìm số mol SO2 sinh ra sau phản ứng
Theo PTHH: 1 mol O2 tham gia phản ứng sinh ra 1 mol SO2
Vậy : 0,125 mol O2 …………………………. 0,125 mol SO2
Tìm thể tích khí SO2(đktc) sinh ra sau phản ứng
VSO2 = n×22,4 = 2,24(l)
Thí dụ 2: tìm thể tích khí oxi (đktc) cần dùng để đốt cháy hoàn toàn 64g lưu huỳnh
Viết PTHH:
S + O2 → SO2 (t0)
Tính số mol lưu huỳnh tham gia phản ứng
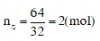
Tính số mol O2 tham gia phản ứng

Theo PTHH: đốt cháy 1 mol S cần dùng 1 mol O2
Vậy : đốt cháy 2 mol S cần 2 mol O2
Tính thể tích O2 cần dùng:
VO2 = 22,4 × n = 44,8 (l)
 [TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
[TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
 Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
 Chào các em lớp 8 yêu dấu ^^, như đã hứa anh sẽ đảm nhiệm giúp đỡ và ôn tập cùng các em trong suốt thời gian sắp tới phục vụ cho kỳ thi HK sắp tới.
Chào các em lớp 8 yêu dấu ^^, như đã hứa anh sẽ đảm nhiệm giúp đỡ và ôn tập cùng các em trong suốt thời gian sắp tới phục vụ cho kỳ thi HK sắp tới.