Mình nhắc lại một chút công thức nhé:
[imath]m=n.M[/imath] => [imath]n = \dfrac{m}{M}[/imath] và [imath]M = \dfrac{m}{n}[/imath]
Với n là số mol, M là khối lượng mol, m là khối lượng
Với chất khí: [imath]V=n.22,4[/imath] => [imath]n=\dfrac{V}{22,4}[/imath]
V là thể tích, n là số mol
Bài 1:
a) [imath]n_{CO}= 0,05 (mol)[/imath]
[imath]n_{CO_2}= 0,15 (mol)[/imath]
=> [imath]m_A= m_{CO} + m_{CO_2} = 1,4 + 6,6 = 8(g)[/imath]
b) [imath]n_A= 0,05 + 0,15 = 0,2 (mol)[/imath]
=> [imath]M_A = \dfrac{8}{0,2} = 40(g/mol)[/imath]
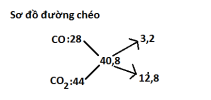
c) [imath]M_B=20,4 .2 = 40,8(g/mol)[/imath]
View attachment 207751
=> tỉ lệ: 3,2/12,8 = 1/4
Còn gì thắc mắc bạn cứ hỏi nhé ^^
Bạn có thể tham khảo thêm các môn học ở đây nha:
TỔNG HỢP kiến thức cơ bản đến nâng cao tất cả các môn
Chúc bạn học tốt

 [TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
[TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
 Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.