- 23 Tháng chín 2018
- 576
- 782
- 161
- TP Hồ Chí Minh
- Đại học sư phạm tphcm
 [TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
[TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
 Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
Tính chất hoá học của Crom – Cr
– Crom là kim loại có tính khử mạnh hơn sắt, có mức oxi hóa từ +1 đến +6, nhưng phổ biến hơn cả là +2, +3, +6.
1. Crom tác dụng với phi kim
– Ở nhiệt độ thường trong không khí, kim loại crôm tạo ra màng mỏng crôm (III) oxit có cấu tạo mịn, bền vững bảo vệ. ở nhiệt độ cao khử được nhiều phi kim.
– Crom tác dụng với Oxi: Cr + O2
4Cr + 3O2 → 2Cr2O3
– Crom tác dụng với Clo: Cr + Cl2
2Cr + 3Cl2 → 2CrCl3
2. Crom tác dụng với nước
– Không tác dụng với nước do có màng oxit bảo vệ.
3. Crom tác dụng với axit
– Với dung dịch axit HCl, H2SO4 loãng nóng, màng axit bị phá huỷ, Cr khử được H+ trong dung dịch axit.
– Crom tác dụng với axit HCl : Cr + HCl
Cr + 2HCl → CrCl2 + H2↑
– Crom tác dụng với axit H2SO4 : Cr + H2SO4
Cr + H2SO4 → CrSO4 + H2↑
– Phương trình ion: 2H+ + Cr → Cr2+ + H2↑
* Lưu ý: Crôm thụ động với axit H2SO4 và HNO3 đặc, nguội.
IV. Hợp chất của Crom (II) – Cr2+
1. Crom (II) Oxit – CrO
– CrO là một oxit bazơ. Màu đen
– CrO có tính khử, trong không khí CrO dễ bị oxi hóa thành Cr2O3.
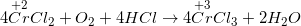
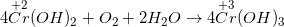
– Dung dịch CrCl2 để ngòai không khí lại chuyển từ màu xanh lam sang màu lục
– CrCl2 trong dung dịch phân ly ra Cr2+ và Cl–. Ion Cr2+ tồn tại ở dạng [Cr(H2O)]2+ có màu xanh, nên dung dịch CrCl2 có màu xanh.
– Mặt khác trạng thái oxi hóa +2 của Cr có tính khử mạnh, ngay trong dung dịch CrCl2 bị oxi hóa bởi oxi không khí chuyển thành CrCl3. Ion Cr3+ trong dung dịch tồn tại duới dạng [Cr(H2O)]3+ có màu lục. Nên trong không khí CrCl2 chuyển từ màu xanh lam sang màu lục.
2. Crom (II) hidroxit – Cr(OH)2
– Cr(OH)2 là chất rắn, màu vàng.
– Cr(OH)2 có tính khử, trong không khí oxi hóa thành Cr(OH)3
– Cr(OH)2 là một bazơ.
3. Muối crom (II)
– Muối crom (II) có tính khử mạnh.
V. Hợp chất của Crom (III) – Cr3+
1. Crom (III) oxit – Cr2O3
– Cr2O3 có cấu trúc tinh thể, mu lục thẫm, có nhiệt độ nóng chảy cao( 22630C)
– Cr2O3 là oxit lưỡng tính, tan trong axit và kiềm đặc.
– Cr2O3 được dùng tạo màu lục cho đồ sứ, đồ thủy tinh.
2. Crom (III) hidroxit – Cr(OH)3
– Cr(OH)3 là hiroxit lưỡng tính, kết tủa nhầy, màu lục nhạt, tan được trong dung dịch axit và dung dịch kiềm.
+ Bị phân huỷ bởi nhiệt tạo oxit tương ứng:
2Cr(OH)3
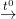 Cr2O3 + 3H2O
Cr2O3 + 3H2O
* Ví dụ 1: Viết các phương trình phản ứng của Cr(OH)3 lần lượt với Na2O2, H2O2, Cl2, Br2, NaOCl, PbO2, KMnO4 trong môi trường kiềm. (Cr3+ bị oxi hoá lên +6).
Cr(OH)3 +3Na2O2 → 2Na2CrO4 + 2NaOH + 2H2O
2Cr(OH)3 + 3H2O2 + 4NaOH → 2Na2CrO4 + 8H2O
2Cr(OH)3 + 3Cl2 + 10 NaOH → 2Na2CrO4 + 6NaCl + 8 H2O
2Cr(OH)3 + 3Br2 + 10NaOH → 2Na2CrO4 + 6NaBr + 8H2O
2Cr(OH)3 + 3NaOCl + 4NaOH → 2Na2CrO4 + 3NaCl + 5H2O
2Cr(OH)3 + 3PbO2 + 4NaOH → 2Na2CrO4 + 3PbO + 5H2O
Cr(OH)3 + 3KmnO4 + 5KOH → K2CrO4 + 3K2MnO4 + 4H2O
* Ví dụ 2: Cho NaOH đến dư vào dung dịch CrCl3, sau đó cho vào dung dịch thu đựợc một ít tinh thể Na2O2, ta có các PTHH của phản ứng:
+ Ban đầu xuất hiện kết tủa keo màu xanh nhạt, lượng kết tủa tăng dần đến cực đại, do phản ứng:
CrCl3 + 3NaOH → Cr(OH)3↓ + 3NaCl
+ Lượng kết tủa tan dần đến hết trong NaOH dư:
Cr(OH)3 + NaOH → NaCrO2 + 2H2O
+ Cho tinh thể Na2O2 vào dung dịch thu được, ta thấy dung dịch xuất hiện màu vàng do tạo muối cromat:
2NaCrO2 + 3Na2O2 + 4H2O → 2Na2CrO4 + 4NaOH
3. Muối crom (III)
– Muối crom (III) có tính khử và tính oxi hóa.
– Muối Cr(III): CrCl3 màu tím, Cr2(SO4)3 màu hồng.
Chú ý: khi vào dung dịch, muối Cr(III) có màu tím-đỏ ở nhiệt độ thường và màu lục khi đun nóng.
– Trong môi trường axit, muối crom (III) có tính oxi hóa bị Zn khử thành muối crom (II)
– Trong môi trường kiềm, muối crom (III) có tính khử và bị chất oxi hóa mạnh oxi hóa thành muối crom (VI).
Phương trình ion:
– Phèn crom-kali K2SO4.Cr2(SO4)3.24H2O có màu xanh tính, được dùng để thuộc da, làm chất cầm màu trong ngành nhuộm vải.
VI. Hợp chất của Crom (VI) – Cr6+
1. Crom (VI) Oxit – CrO3
– CrO3 là chất oxi hóa rất mạnh. Một số chất vô cơ và hữu cơ như S, P, C, NH3, C2H5OH,… bốc cháy khi tiếp xúc với CrO3, CrO3 bị khử thành Cr2O3.
– CrO3 là oxit axit, khi tác dụng với nước tạo thành hỗn hợp axit cromic H2CrO4 và axit đicromic H2Cr2O7. Hai axit này không thể tách ra ở dạng tự do, chỉ tồn tại trong dung dịch. Nếu tách ra khỏi dung dịch, chúng bị phân hủy thành CrO3.
2. Muối cromat và đicromat
– Ion cromat CrO42- có màu vàng. Ion đicromat Cr2O7 2- có màu da cam.
– Trong môi trường axit, cromat (màu vàng), chuyển hóa thành đicromat.(màu da cam)
– Trong môi trường kiềm đicromat.(màu da cam), chuyển hóa thành cromat (màu vàng)
* Tổng quát:
– Muối cromat và đicromat có tính oxi hóa mạnh, chúng bị khử thành muối Cr (III).
– (NH4)2Cr2O7 bị nhiệt phân theo phản ứng:
(NH4)2Cr2O7
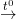 Cr2O3 + N2↑ + 4H2O
Cr2O3 + N2↑ + 4H2O
– Phèn Crom : Cr2(SO4)3.K2SO4.24H2O
Cr2(SO4)3 + 6KOH → 2Cr(OH)3 + 3K2SO4
2Cr(OH)3 + 3Br2 + 10KOH → 2K2CrO4 + 6KBr + 8H2O.
2K2CrO4 + H2SO4 → K2Cr2O7 + K2SO4
K2Cr2O7 + H2SO4 đặc → CrO3 + K2SO4 + H2O
– Crom là kim loại có tính khử mạnh hơn sắt, có mức oxi hóa từ +1 đến +6, nhưng phổ biến hơn cả là +2, +3, +6.
1. Crom tác dụng với phi kim
– Ở nhiệt độ thường trong không khí, kim loại crôm tạo ra màng mỏng crôm (III) oxit có cấu tạo mịn, bền vững bảo vệ. ở nhiệt độ cao khử được nhiều phi kim.
– Crom tác dụng với Oxi: Cr + O2
4Cr + 3O2 → 2Cr2O3
– Crom tác dụng với Clo: Cr + Cl2
2Cr + 3Cl2 → 2CrCl3
2. Crom tác dụng với nước
– Không tác dụng với nước do có màng oxit bảo vệ.
3. Crom tác dụng với axit
– Với dung dịch axit HCl, H2SO4 loãng nóng, màng axit bị phá huỷ, Cr khử được H+ trong dung dịch axit.
– Crom tác dụng với axit HCl : Cr + HCl
Cr + 2HCl → CrCl2 + H2↑
– Crom tác dụng với axit H2SO4 : Cr + H2SO4
Cr + H2SO4 → CrSO4 + H2↑
– Phương trình ion: 2H+ + Cr → Cr2+ + H2↑
* Lưu ý: Crôm thụ động với axit H2SO4 và HNO3 đặc, nguội.
IV. Hợp chất của Crom (II) – Cr2+
1. Crom (II) Oxit – CrO
– CrO là một oxit bazơ. Màu đen
– CrO có tính khử, trong không khí CrO dễ bị oxi hóa thành Cr2O3.
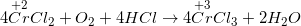
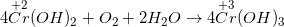
– Dung dịch CrCl2 để ngòai không khí lại chuyển từ màu xanh lam sang màu lục
– CrCl2 trong dung dịch phân ly ra Cr2+ và Cl–. Ion Cr2+ tồn tại ở dạng [Cr(H2O)]2+ có màu xanh, nên dung dịch CrCl2 có màu xanh.
– Mặt khác trạng thái oxi hóa +2 của Cr có tính khử mạnh, ngay trong dung dịch CrCl2 bị oxi hóa bởi oxi không khí chuyển thành CrCl3. Ion Cr3+ trong dung dịch tồn tại duới dạng [Cr(H2O)]3+ có màu lục. Nên trong không khí CrCl2 chuyển từ màu xanh lam sang màu lục.
2. Crom (II) hidroxit – Cr(OH)2
– Cr(OH)2 là chất rắn, màu vàng.
– Cr(OH)2 có tính khử, trong không khí oxi hóa thành Cr(OH)3
– Cr(OH)2 là một bazơ.
3. Muối crom (II)
– Muối crom (II) có tính khử mạnh.
V. Hợp chất của Crom (III) – Cr3+
1. Crom (III) oxit – Cr2O3
– Cr2O3 có cấu trúc tinh thể, mu lục thẫm, có nhiệt độ nóng chảy cao( 22630C)
– Cr2O3 là oxit lưỡng tính, tan trong axit và kiềm đặc.
– Cr2O3 được dùng tạo màu lục cho đồ sứ, đồ thủy tinh.
2. Crom (III) hidroxit – Cr(OH)3
– Cr(OH)3 là hiroxit lưỡng tính, kết tủa nhầy, màu lục nhạt, tan được trong dung dịch axit và dung dịch kiềm.
+ Bị phân huỷ bởi nhiệt tạo oxit tương ứng:
2Cr(OH)3
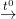
* Ví dụ 1: Viết các phương trình phản ứng của Cr(OH)3 lần lượt với Na2O2, H2O2, Cl2, Br2, NaOCl, PbO2, KMnO4 trong môi trường kiềm. (Cr3+ bị oxi hoá lên +6).
Cr(OH)3 +3Na2O2 → 2Na2CrO4 + 2NaOH + 2H2O
2Cr(OH)3 + 3H2O2 + 4NaOH → 2Na2CrO4 + 8H2O
2Cr(OH)3 + 3Cl2 + 10 NaOH → 2Na2CrO4 + 6NaCl + 8 H2O
2Cr(OH)3 + 3Br2 + 10NaOH → 2Na2CrO4 + 6NaBr + 8H2O
2Cr(OH)3 + 3NaOCl + 4NaOH → 2Na2CrO4 + 3NaCl + 5H2O
2Cr(OH)3 + 3PbO2 + 4NaOH → 2Na2CrO4 + 3PbO + 5H2O
Cr(OH)3 + 3KmnO4 + 5KOH → K2CrO4 + 3K2MnO4 + 4H2O
* Ví dụ 2: Cho NaOH đến dư vào dung dịch CrCl3, sau đó cho vào dung dịch thu đựợc một ít tinh thể Na2O2, ta có các PTHH của phản ứng:
+ Ban đầu xuất hiện kết tủa keo màu xanh nhạt, lượng kết tủa tăng dần đến cực đại, do phản ứng:
CrCl3 + 3NaOH → Cr(OH)3↓ + 3NaCl
+ Lượng kết tủa tan dần đến hết trong NaOH dư:
Cr(OH)3 + NaOH → NaCrO2 + 2H2O
+ Cho tinh thể Na2O2 vào dung dịch thu được, ta thấy dung dịch xuất hiện màu vàng do tạo muối cromat:
2NaCrO2 + 3Na2O2 + 4H2O → 2Na2CrO4 + 4NaOH
3. Muối crom (III)
– Muối crom (III) có tính khử và tính oxi hóa.
– Muối Cr(III): CrCl3 màu tím, Cr2(SO4)3 màu hồng.
Chú ý: khi vào dung dịch, muối Cr(III) có màu tím-đỏ ở nhiệt độ thường và màu lục khi đun nóng.
– Trong môi trường axit, muối crom (III) có tính oxi hóa bị Zn khử thành muối crom (II)
– Trong môi trường kiềm, muối crom (III) có tính khử và bị chất oxi hóa mạnh oxi hóa thành muối crom (VI).
Phương trình ion:
– Phèn crom-kali K2SO4.Cr2(SO4)3.24H2O có màu xanh tính, được dùng để thuộc da, làm chất cầm màu trong ngành nhuộm vải.
VI. Hợp chất của Crom (VI) – Cr6+
1. Crom (VI) Oxit – CrO3
– CrO3 là chất oxi hóa rất mạnh. Một số chất vô cơ và hữu cơ như S, P, C, NH3, C2H5OH,… bốc cháy khi tiếp xúc với CrO3, CrO3 bị khử thành Cr2O3.
– CrO3 là oxit axit, khi tác dụng với nước tạo thành hỗn hợp axit cromic H2CrO4 và axit đicromic H2Cr2O7. Hai axit này không thể tách ra ở dạng tự do, chỉ tồn tại trong dung dịch. Nếu tách ra khỏi dung dịch, chúng bị phân hủy thành CrO3.
2. Muối cromat và đicromat
– Ion cromat CrO42- có màu vàng. Ion đicromat Cr2O7 2- có màu da cam.
– Trong môi trường axit, cromat (màu vàng), chuyển hóa thành đicromat.(màu da cam)
– Trong môi trường kiềm đicromat.(màu da cam), chuyển hóa thành cromat (màu vàng)
* Tổng quát:
– Muối cromat và đicromat có tính oxi hóa mạnh, chúng bị khử thành muối Cr (III).
– (NH4)2Cr2O7 bị nhiệt phân theo phản ứng:
(NH4)2Cr2O7
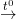
– Phèn Crom : Cr2(SO4)3.K2SO4.24H2O
Cr2(SO4)3 + 6KOH → 2Cr(OH)3 + 3K2SO4
2Cr(OH)3 + 3Br2 + 10KOH → 2K2CrO4 + 6KBr + 8H2O.
2K2CrO4 + H2SO4 → K2Cr2O7 + K2SO4
K2Cr2O7 + H2SO4 đặc → CrO3 + K2SO4 + H2O

