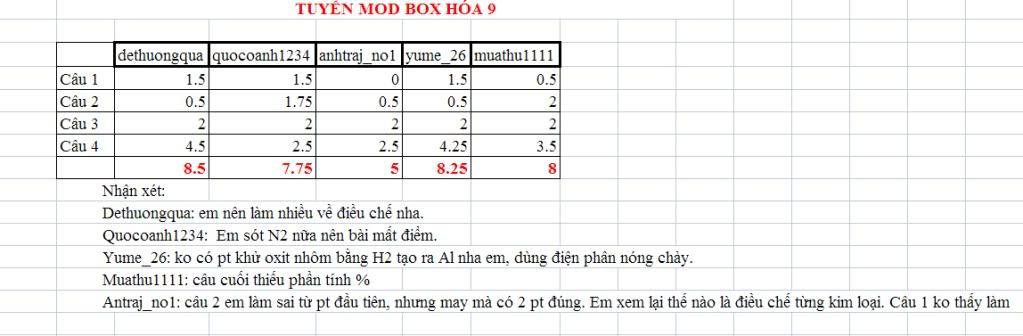
Bài làm của các mem
quocoanh12345
http://www.mediafire.com/?odq3dnqpfuvf6dj
yumi_26
1. [TEX] m_T = 2 - 0,9 = 1,1 (g) [/TEX]
\Rightarrow [TEX] M_T = 1,1 : 0,025 = 44 (g) [/TEX]
\Rightarrow T là N2O (CO2 ko thỏa mãn đề bài)
[TEX] n_{H_2O} = 0,9 : 18 = 0,05 (mol) [/TEX]
\Rightarrow [TEX] \frac{n_{H_2O}}{n_{N_2O}} = \frac{0,05}{0,025} = \frac{2}{1} [/TEX]
\Rightarrow CT của Y có dạng [TEX] H_4N_2O_3 [/TEX]
\Rightarrow CT của muối: [TEX] NH_4NO_3 [/TEX]
\Rightarrow 2 chất ban đầu: [TEX] M(NO_3)_2 ; (NH_4)_aA [/TEX]
[TEX] M(NO_3)_2 + (NH_4)_aA \rightarrow \ X \downarrow \ + NH_4NO_3[/TEX]
Từ PƯ [TEX] NH_4NO_3 \rightarrow \ N_2O + 2H_2O [/TEX]
\Rightarrow [TEX] n_{NH_4NO_3} = n_{N_2O} = 0,025 mol [/TEX]
[TEX] aM(NO_3)_2 \rightarrow \ 2aNH_4NO_3 [/TEX]
\Rightarrow [TEX] n_{M(NO_3)_2} = n_{NH_4NO_3} . 0,5 = 0,025 . 0,5 = 0,0125 (mol) [/TEX]
[TEX] M(NO_3)_2 \rightarrow \ X \rightarrow \ MO [/TEX]
\Rightarrow [TEX] n_{MO} = n_{X} = n_{M(NO_3)_2} = 0,0125 (mol) [/TEX]
\Rightarrow [TEX] M_{MO} = 0,7 : 0,0125 = 56 (g) [/TEX]
\Rightarrow M = 40 \Rightarrow CTHH MO là CaO
[TEX] m_Z = 1,25 - 0,7 = 0,55 (g) [/TEX]
Đặt Z = BxOy
\Rightarrow [TEX] n_{B_xO_y} = n_{CaO} = 0,0125 (mol) [/TEX]
\Rightarrow [TEX] M_{B_xO_y} = 0,55 : 0,0125 = 44 (g) [/TEX]
\Rightarrow Z là CO2
\Rightarrow X là CaCO3
[TEX] CaCO_3 \Large\longrightarrow^{\text{t^o}} CaO + CO_2 [/TEX]
Vậy 2 muối ban đầu là [TEX] Ca(NO_3)_2 [/TEX] và [TEX] (NH_4)_2CO_3 [/TEX]
[TEX] Ca(NO_3)_2 + (NH_4)_2CO_3 \rightarrow \ CaCO_3 \downarrow \ + 2NH_4NO_3[/TEX]
2. Cho hỗn hợp t/dụng với dd NaOH dư. Chỉ có Al2O3 phản ứng tạo kết tủa:
[TEX] Al_2O_3 + 2NaOH \rightarrow \ 2NaAlO_2 + H_2O [/TEX]
[TEX] 2NaAlO_2 + 2CO_2 + 4H_2O \rightarrow \ Al(OH)_3 + NaHCO_3[/TEX]
Nung Al(OH)3:
[TEX] Al(OH)_3 \Large\longrightarrow^{\text{t^o}} Al_2O_3 + 3H_2O [/TEX]
Dẫn khí H2 thu đc Al:
[TEX] Al_2O_3 + 3H_2 \Large\longrightarrow^{\text{t^o}} 2Al + 3H_2O[/TEX]
3.
1. [TEX] 4FeS_2 + 11O_2 \Large\longrightarrow^{\text{t^0}} 8SO_2 \uparrow \ + 2Fe_2O_3 [/TEX]
2. [TEX] SO_2 + H_2S \rightarrow \ 3S \downarrow \ 2H_2O [/TEX]
3. [TEX] S + Fe \Large\longrightarrow^{\text{t^0}} FeS [/TEX]
4. [TEX] FeCl_2 + 2NaOH \rightarrow \ Fe(OH)_2 \downarrow \ + 2NaCl [/TEX]
5. [TEX] 2Fe(OH)_3 \Large\longrightarrow^{\text{t^0}} Fe_2O_3 + 3H_2O [/TEX]
6. [TEX] Fe_O_3 + 3H_2 \Large\longrightarrow^{\text{t^0}} 2Fe + 3H_2O [/TEX]
7. [TEX] FeS + 2HCl \rightarrow \ FeCl_2 + H_2S [/TEX]
8. [TEX] Fe(OH)_2 + O_2 + H_2O \rightarrow \ Fe(OH)_3 \downarrow \ [/TEX]
A: SO2; B: Fe2O3; C: S ; D: H2O; E: Fe; F: FeS
4. a) Gọi A là CTHH chung cho 2 kim loại. Đặt A là khối lượng mol trung bình của A.
[TEX] ACO_3 + 2HNO_3 \rightarrow \ A(NO_3)_2 + H_2O + CO_2 \uparrow \[/TEX]
[TEX] n_{BaCO_3} = 7,88 : 197 = 0,04(mol) [/TEX]
[TEX] CO_2 + Ba(OH)_2 \rightarrow \ BaCO_3 \downarrow \ + H_2O[/TEX]
0,04 mol <-- ...................... 0,04 mol
[TEX] ACO_3 + 2HNO_3 \rightarrow \ A(NO_3)_2 + CO_2 \uparrow \ + H_2O[/TEX]
0,04mol <--- .........................0,04 mol
\Rightarrow 0,04.(A + 60) = 3,6
\Leftrightarrow 0,04A + 2,4 = 3,6
\Leftrightarrow A = 30
\Rightarrow 24< A < 40
Vậy 2 kim loại của 2 muối là Mg và Ca
\Rightarrow CTHH của 2 muối: [TEX] MgCO_3; CaCO_3 [/TEX]
Gọi a, b lần lượt là số mol của 2 muối MgCO3 và CaCO3.
[TEX] MgCO_3 + 2HNO_3 \rightarrow \ Mg(NO_3)_2 + CO_2 + H_2O [/TEX]
a mol ................................-->.................. a mol
[TEX] CaCO_3 + 2HNO_3 \rightarrow \ Ca(NO_3)_2 + CO_2 + H_2O [/TEX]
b mol ....................................................--> b mol
[TEX] \Rightarrow \left{\begin{84a + 100b = 3,6}\\{a + b = 0,04}[/TEX]
Giải hệ ta có a = 0,025; b = 0,015
\Rightarrow [TEX] m_{MgCO_3} = 0,025 . 84 = 2,1(g) [/TEX]
\Rightarrow [TEX] %MgCO_3 = \frac{2,1 . 100%}{3,6} = 58,33%[/TEX]
\Rightarrow [TEX] %CaCO_3 = 100% - 58,33% = 41,67% [/TEX]
b) Trong 3,6g hỗn hợp X chứa 2,1g MgCO3
\Rightarrow trong 7,2g hỗn hợp X chứa 4,2g MgCO3
\Rightarrow [TEX] n_{MgCO_3} = 4,2 : 84 = 0,05 (mol) [/TEX]
\Rightarrow [TEX] n_{CaCO_3} = 0,03 (mol) [/TEX]
[TEX] n_{FeCO_3} = 6,96 : 116 = 0,06 (mol) [/TEX]
[TEX] MgCO_3 \Large\longrightarrow^{\text{t^0}} CO_2 + MgO [/TEX]
0,05mol .......---> 0,05 mol .....---> 0,05 mol
[TEX] CaCO_3 \Large\longrightarrow^{\text{t^0}} CO_2 + CaO [/TEX]
0,03 mol ..........--> 0,03 mol ............--> 0,03 mol
[TEX] FeCO_3 \Large\longrightarrow^{\text{t^0}} CO_2 + FeO [/TEX]
0,06 mol .....--> 0,06 mol .......---> 0,06 mol
\Rightarrow [TEX] \sum n_{CO_2} = 0,05 + 0,03 + 0,06 = 0,14 (mol) [/TEX]
[TEX] n_{kk} = 5,6 : 22,4 = 0,25 (mol) [/TEX]
\Rightarrow [TEX] n_O_2 = 0,25 . \frac{1}{5} = 0,05 (mol) [/TEX]; [TEX] n_N_2 = 0,25 - 0,05 = 0,2 (mol) [/TEX]
\Rightarrow [TEX] % n_{CO_2} = \frac{0,14 . 100%}{0,25 + 0,14} = 35,9 %[/TEX]
[TEX] % n_{O_2} = \frac{0,05 . 100%}{0,25 + 0,14} = 12,8% [/TEX]
[TEX] % n_{N_2} = \frac{0,2 . 100%}{0,25 + 0,14} = 51,3%[/TEX]
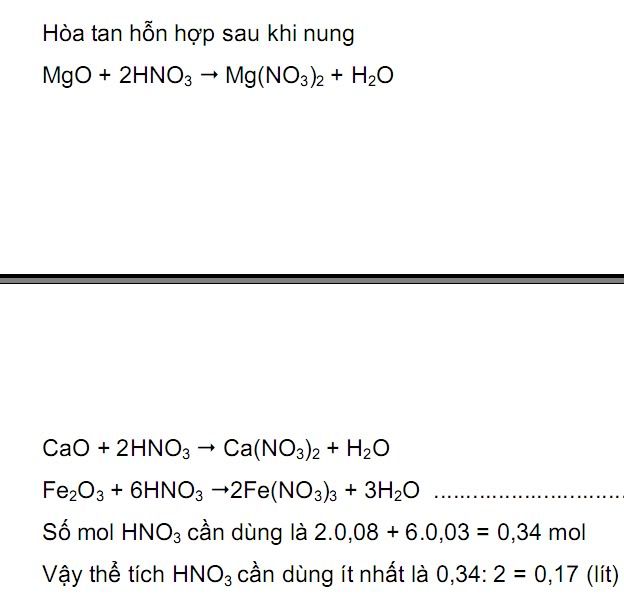
c) [TEX] MgO + 2HNO_3 \rightarrow \ Mg(NO_3)_2 + H_2O [/TEX]
0,05 mol ---> 0,1 mol
[TEX] CaO + 2HNO_3 \rightarrow \ Ca(NO_3)_2 + H_2O [/TEX]
0,03 mol ---> 0,06 mol
[TEX] 3FeO + 10HNO_3 \rightarrow \ 3Fe(NO_3)_3 + NO + 5H_2O[/TEX]
0,06 mol ----> 0,2mol
\Rightarrow [TEX] \sum n_{HNO_3} = 0,1 + 0,06 + 0,2 = 0,36 (mol) [/TEX]
\Rightarrow [TEX] V_{HNO_3} = 0,36 : 2 = 0,18 (l) [/TEX][/QUOTE][/QUOTE]
 [TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
[TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
 Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.