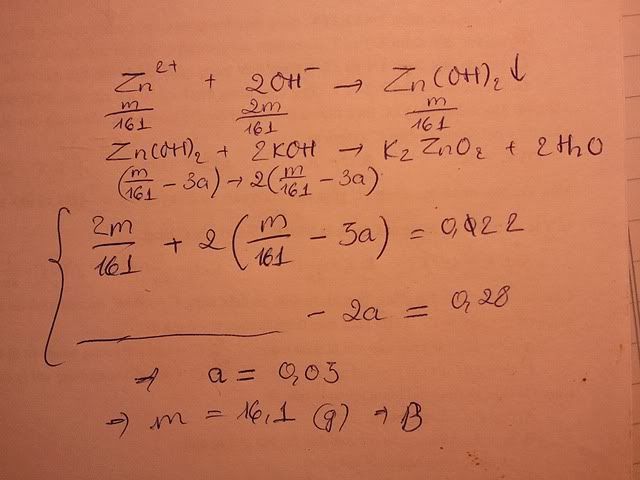N
newyork15992
 [TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
[TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
 Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
Mình thắc mắc một số câu trong đề thi năm ngoái , có bạn nào giải giúp với:
C1 Hoà tan hoàn toàn m gam ZnSO4 vào nước được dung dịch X .Nếu cho 110ml dung dịch KOH 2M vào X thì thu được 3a gam kết tủa .Mặt khác nếu cho 140ml dung dịch KOH 2M vào X thì thu được 2a gam kết tủa . Giá trị của m là ?
A.17,71
B.16,10
C.32,2
D.24,15
C2.Cho dung dịch X gồm :0,007mol Na+ , 0,003mol Ca2+ ,0,006mol Cl- ,0,006mol HCO3- và 0,001mol NO3- .Để loại bỏ hết Ca2+ trong X cần 1 lượng vừa đủ dung dịch chứa a gam Ca(OH)2 . Giá trị của a là ?
A.0,18
B.0,12
C.0,444
D.0,222
C3.Cho m gam NaOH vào 2 lít dung dịch NaHCO3 nồng độ a mol/l , thu được 2 lít dung dịch X. Lấy 1 lít dung dịch X tác dụng với dung dịch BaCl2 (dư)thu được 11,82gam kết tủa .Mặt khác ,cho 1 lít dung dịch X vào dung dịch CaCl2 dư rồi đun nóng , sau khi phản ứng kết thúc thu được 7g kết tủa . Giá trị của a và m tương ứng la`
A.0,08 và 4,8
B.0,04 và 4,8
C.0,14 và 2,4
D.0,07 và 3,2
Các bạn giải chi tiết giúp mình nhé. Thanks
C1 Hoà tan hoàn toàn m gam ZnSO4 vào nước được dung dịch X .Nếu cho 110ml dung dịch KOH 2M vào X thì thu được 3a gam kết tủa .Mặt khác nếu cho 140ml dung dịch KOH 2M vào X thì thu được 2a gam kết tủa . Giá trị của m là ?
A.17,71
B.16,10
C.32,2
D.24,15
C2.Cho dung dịch X gồm :0,007mol Na+ , 0,003mol Ca2+ ,0,006mol Cl- ,0,006mol HCO3- và 0,001mol NO3- .Để loại bỏ hết Ca2+ trong X cần 1 lượng vừa đủ dung dịch chứa a gam Ca(OH)2 . Giá trị của a là ?
A.0,18
B.0,12
C.0,444
D.0,222
C3.Cho m gam NaOH vào 2 lít dung dịch NaHCO3 nồng độ a mol/l , thu được 2 lít dung dịch X. Lấy 1 lít dung dịch X tác dụng với dung dịch BaCl2 (dư)thu được 11,82gam kết tủa .Mặt khác ,cho 1 lít dung dịch X vào dung dịch CaCl2 dư rồi đun nóng , sau khi phản ứng kết thúc thu được 7g kết tủa . Giá trị của a và m tương ứng la`
A.0,08 và 4,8
B.0,04 và 4,8
C.0,14 và 2,4
D.0,07 và 3,2
Các bạn giải chi tiết giúp mình nhé. Thanks