 [TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
[TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
 Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
Chuyên đề: Tách chất hoá học
Khi sử dụng phương pháp hoá học để tách hoặc tinh chế hoá chất vô cơ cần lưu ý các điều kiện sau:1. Phản ứng để tách riêng hoá chất ra khỏi hỗn hợp phải có đủ 3 điều kiện:
- Chỉ tác dụng lên một chất trong hỗn hợp (thường là chất muốn tách).
- Sản phẩm tạo thành có thể tách dễ dàng ra khỏi hỗn hợp như: kết tủa, tạo 2 dung dịch không tan vào nhau.
- Từ sản phẩm tạo thành để tái tạo lại chất bạn đầu.
2. Các dạng bài tập tách thường gặp
a, Tách riêng một chất ra khỏi hỗn hợp (tinh thể chất)
Ví dụ: Bằng phương pháp hoá học, tách Ag ra khỏi hỗn hợp Cu; Fe; Ag
b, Tách riêng từng chất ra khỏi hỗn hợp.
Ví dụ: Bằng phương pháp hoá học tách riêng từng chất ra khỏi hỗn hợp gồm: Cu, Fe, Ag.
3. Phương pháp làm bài tập tách chất
a, Phương pháp loại bỏ: phương pháp này dùng để tách một chất ra khỏi hỗn hợp khi chất cần tách khó hoặc không tham gia phản ứng hoá học.
+, Sơ đồ tổng quát: có hỗn hợp A, B. Ta muốn tách A:
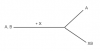
(Sơ đồ trên cho thấy: Khi có hỗn hợp A, B. Muốn tách A, ta cho hỗn hợp trên tác dụng với chất X, đảm bảo chỉ có X phản ứng với B tạo XB, còn lại thu được A).
Ví dụ: Để tách $N_2$ ra khỏi hỗn hợp gồm: $N_2; CO_2; H_2; CO$ ta dẫn hỗn hợp A qua bình đựng chưa CuO dư (nhiệt độ cao), bình 2 đựng dung dịch $Ca(OH)_2$ dư, bình 3 đựng dung dịch $H_2SO_4$ đặc. Thu khí thoát ra khỏi bình là $N_2$ tinh khiết.
Chú ý: Trong ví dụ trên, nhận thấy $N_2$ là chất khí không tham gia phản ứng với $CuO; NaOH; H_2SO_4$ nên ta thu khí này bằng phương pháp loại bỏ.
b, Phương pháp tái tạo: Dùng để tách các chất dễ tham gia các phản ứng hoá học với một chất trong khi các chất khác trong hỗn hợp không phản ứng.
+, Sơ đồ tổng quát: Có hỗn hợp X, Y. Ta muốn tách Y
(Sơ đồ trên cho thấy: Khi có hỗn hợp X, Y, muốn tách Y ta cho hỗn hợp trên phản ứng với chất A, đảm bảo chỉ có Y phản ứng với A tạo ra YA, từ YA ta lại tái tạo lại được Y).
Ví dụ: Để tách $CO_2$ ra khỏi hỗn hợp A (trong ví dụ 1), ta dẫn hỗn hợp A qua bình đựng dung dịch $Ca(OH)_2$ dư, $CO_2$ bị giữ lại do phản ứng:
[tex]CO_2+Ca(OH)_2\rightarrow CaCO_3+H_2O[/tex]
Lọc lấy kết tủa nung đến khối lượng không đổi thu được $CO_2$:
[tex]CaCO_3\overset{t^o}{\rightarrow}CaO+CO_2[/tex]
Như vậy ta đã chuyển $CO_2$ thành một chất không tan là $CaCO_3$ rồi từ đó tái tạo lại chúng nhờ phản ứng phân huỷ.
@Hồng Nhật

