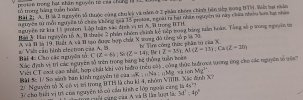Các anh chị giúp e bài 2 3 4 5 với ạ e cảm ơn ạ
Phuongg Ahn5.1 Bán kính nguyên tử:
+ Trong chu kì, theo chiều tăng của điện tích hạt nhân, bán kính nguyên tử giảm dần, vì số electron ngoài cùng tăng dần trong khi số lớp electron không thay đổi.
+ Trong nhóm A, theo chiều tăng của điện tích hạt nhân, bán kính nguyên tử tăng dần, do số lớp electron tăng dần.
=> Bán kính Mg < Na < K
- Mặt khác [imath]Mg ^{2+}[/imath] < Mg
Cả nguyên tử Mg và ion [imath]Mg ^{2+}[/imath] đều có điện tích hạt nhân là 12+. Mà nguyên tử Mg có 12 electron còn ion [imath]Mg ^{2+}[/imath] có 10 electron nên hạt nhân của ion [imath]Mg ^{2+}[/imath] sẽ hút các electron mạnh hơn làm cho bán kính ion nhỏ hơn
=> [imath]Mg ^{2+}[/imath] < Mg < Na < K
5.2 X thuộc nhóm VIIIB → Electron cuối cùng điền vào phân lớp d, X có 8, 9 hoặc 10 electron hóa trị và X thuộc chu kì 4 => X có thể là các nguyên tố Fe, Co, Ni
5.3. Sẽ có 3 nguyên tố với CT như sau thỏa
[imath]1s^{2}2s^{2}2p^{6}3s^{2}3p^{6}4s^{1}[/imath]
[imath]1s^{2}2s^{2}2p^{6}3s^{2}3p^{6}3d^{5}4s^{1}[/imath] (bán bảo toàn)
[imath]1s^{2}2s^{2}2p^{6}3s^{2}3p^{6}3d^{10}4s^{1}[/imath]
Note: Nếu đề cho nguyên tử của nguyên tố X có electron cuối cùng được điền vào phân lớp [imath]4s^{1}[/imath]
=> cấu hình e: [imath][Ar]4s^{1}[/imath]
Bên mình sẽ cố gắng hỗ trợ các câu còn lại sớm nhất có thể cho bạn nha ^ ^
Bạn còn thắc mắc gì thì ghi bên dưới nhé ^ ^
Bạn tham khảo BT có giải tương tự tại đây nha:
Bảng tuần hoàn
 [TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
[TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
 Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.