- 25 Tháng mười 2018
- 1,560
- 1,684
- 251
- 29
- Quảng Bình
- Đại học Sư phạm Huế
 [TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
[TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
 Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
ẢNH HƯỞNG CỦA CẤU TẠO TỚI TÍNH CHẤT HÓA HỌC
Cấu tạo có ảnh hưởng lớn tới tính chất vật lí và tính chất hóa học của các chất. Ở bài viết hôm nay mình sẽ viết về sự ảnh hưởng của cấu tạo tới tính chất của các hợp chất vô cơ.+ Khi học bài Nitơ, chắc hẳn các bạn thấy trong SGK có viết N2 trơ về mặt hóa học, chỉ tác dụng với các chất ở nhiệt độ cao. Vì sao lại như thế?
N: 1s22s22p3
Nguyên tử N có 5e lớp ngoài cùng, cần thêm 3e để đạt cấu hình bền của khí hiếm với 8e lớp ngoài cùng ⇒ mỗi nguyên tử N góp chung 3e tạo phân tử N2 trong đó 2 nguyên tử N liên kết với nhau bằng liên kết 3 bền vững.
N2: N≡N
Tưởng tượng liên kết hóa học đơn như 1 chiếc đũa ⇒ liên kết 3 là 3 chiếc đũa mà việc bẻ gãy 3 chiếc đũa khó hơn so với việc bẻ gãy 1 chiếc đũa.
Như vậy có thể thấy việc bẻ gãy liên kết ba khó khăn ⇒ Ở điều kiện thường thì nitơ trơ về mặt hóa học.
+ Chắc hẳn nhiều bạn thắc mắc vì sao H3PO4 là axit 3 nấc trong khi đó H3PO3 là axit 2 nấc và H3PO2 là axit 1 nấc trong khi đó chúng đều có 3 nguyên tử H.
Cấu tạo:
H phải liên kết với nguyên tử có độ âm điện lớn thì nguyên tử H mới linh động ⇒ H đó có tính axit
Từ cấu tạo ta có thể thấy:
H3PO4: có 3 nguyên tử H liên kết trực tiếp với nguyên tử O ⇒ 3 nguyên tử H linh động ⇒ Axit 3 nấc
H3PO3: có 2 nguyên tử H liên kết trực tiếp với nguyên tử O ⇒ 2 nguyên tử H linh động ⇒ Axit 2 nấc
H3PO2: có 1 nguyên tử H liên kết trực tiếp với nguyên tử O ⇒ 1 nguyên tử H linh động ⇒ Axit 1 nấc.
Tương tự từ cấu tạo của các axit HCl, H2SO4, HNO3, … bạn có thể giải thích được vì sao chúng là những axit mạnh.
Tại sao H2SO4 đặc lại có tính oxi hóa mạnh, trong khi H2SO4 loãng chỉ thể hiện tính axit ?
Cấu tạo H2SO4
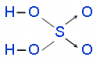
Trong H2SO4 thì S có số oxi hóa +6 đây là số oxi hóa cao nhất của S
Dựa vào cấu tạo thì ta có thể thấy
Phân tử H2SO4 có cấu tạo bất đối xứng ⇒ cấu tạo bất đối xứng thì kém bền nên H2SO4 có tính oxi hóa mạnh.
H2SO4 đặc thì H2SO4 chủ yếu tồn tại ở dạng phân tử.
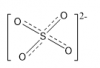
H2SO4 loãng thì H2SO4 sẽ phân li cho H+ và ion SO42-
Nhìn vào cấu tạo của SO42- có thể thấy mặc dù S mang số oxi hóa +6 nhưng do cấu tạo của ion SO42- đối xứng nên rất bền vững vì vậy không thể hiện tính oxi hóa.
⇒ H2SO4 đặc có tính oxi hóa mạnh, H2SO4 loãng chỉ thể hiện tính axit.
Tương tự như vậy, các bạn dựa vào cấu tạo để suy luận và giải thích:
1. Vì sao HNO3 có tính oxi hóa mạnh ?
2. Vì sao NH3 có tính bazơ ?
3. Tính axit tăng dần từ HF → HI, giải thích?

