- 25 Tháng mười 2018
- 1,560
- 1,684
- 251
- 29
- Quảng Bình
- Đại học Sư phạm Huế
 [TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
[TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
 Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
Đốt cháy amin CxHyNt

Phương pháp giải:
- Bảo toàn nguyên tố : nO2 pứ = nCO2 + 0,5.nH2O
- Bảo toàn khối lượng: mCxHyNt = mC + mH + mN = 12.nCO2 + 2.nH2O + 14.2nN2
Lưu ý: Khi đốt cháy 1 amin ngoài không khí: nN2 sau pứ = nN2 (tạo ra từ pứ cháy) + nAmin
Câu 1 (ĐHKA-2007): Khi đốt cháy hoàn toàn một amin đơn chức X, thu được 8,4 (l) CO2, 1,4 (l) N2 (các thể tích đo ở đktc) và 10,125g H2O. Công thức phân tử của X là?
A. C3H7N B. C2H7N C. C3H9N D. C4H9N
Giải: nCO2 = 0,375 mol; nH2O = 0,5625 mol; nN2 = 0,0625 mol
Cách 1: Tìm CTPT dựa vào CTĐGN
nC : nH : nN = nCO2 : 2nH2O : 2nN2 = 0,375 : 0,5625.2 : 0,0625.2 = 3 : 9 : 1
⇒ X có CTPT là (C3H9N)n
Vì X là amin đơn chức nên n = 1 ⇒ Vậy CTPT của X là C3H9N
Cách 2: Thiết lập CTPT:
nAmin = 2.nN2 = 0,125 mol
Số C = nCO2/nAmin = 3; Số H = 2.nH2O/nAmin = 9; Số N = 2.nN2/nAmin = 1
Vậy amin là C3H7N.
Câu 2: Đốt cháy hoàn toàn hỗn hợp 2 amin no, đơn chức, là đồng đẳng liên tiếp, thu được 2,24 lít khí CO2 (đktc) và 3,6 gam H2O. Công thức phân tử của 2 amin là:
A. CH5N và C2H7N B. C2H7N và C3H9N C. C3H9N và C4H11N D. Kết quả khác
Giải: Amin no, đơn chức có CTTQ là CnH2n+3N
Ta có: nCO2 = 0,1 mol; nH2O = 0,2 mol
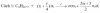
Ta có: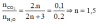
2 amin đồng đẳng kết tiếp ⇒ 2 amin là CH5N và C2H7N
Cách 2: Với amin no, đơn chức, mạch hở ta có: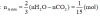
Số nguyên tử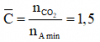 ⇒ 2 amin đồng đẳng kế tiếp là CH5N và C2H7N
⇒ 2 amin đồng đẳng kế tiếp là CH5N và C2H7N
Câu 3: Đốt cháy amin A với không khí (N2 và O2 với tỷ lệ mol 4:1) vừa đủ, sau phản ứng thu được 17,6g CO2; 12,6g H2O và 69,44 lít N2 (đktc). Khối lượng của amin là?
A. 9,2g B. 9g C. 11g D. 9,5g
Giải: nCO2 = 0,4 mol; nH2O = 0,7 mol; nN2 = 3,1 mol
Bảo toàn nguyên tố O: 2.nO2 = 2.nCO2 + nH2O ⇒ nO2 = 0,75 mol
Vậy nN2 (kk) = 4.nO2 = 3 mol
⇒ nN2 (pứ cháy) = nN2 – nN2(kk) = 0,1 mol
mAmin = 12.nCO2 + 2.nH2O + 28.nN2 = 9 gam
Câu 4: Đốt cháy hoàn toàn 0,1mol hỗn hợp gồm metylamin, đimetylamin, trimetylamin và etylamin bằng oxi vừa đủ thì thể tích N2 thu được (ở đktc) là
A. 4,48 lít B. 2,24 lít C. 1,12 lít D. 3,36 lít
Giải: Metylamin, đimetylamin; trimetyamin đều là amin đơn chức
⇒ Đặt công thức chung của amin là CxHyN.
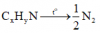
⇒ nN2 = 0,5.nAmin = 0,05 mol ⇒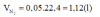
Phương pháp giải:
- Bảo toàn nguyên tố : nO2 pứ = nCO2 + 0,5.nH2O
- Bảo toàn khối lượng: mCxHyNt = mC + mH + mN = 12.nCO2 + 2.nH2O + 14.2nN2
Lưu ý: Khi đốt cháy 1 amin ngoài không khí: nN2 sau pứ = nN2 (tạo ra từ pứ cháy) + nAmin
Câu 1 (ĐHKA-2007): Khi đốt cháy hoàn toàn một amin đơn chức X, thu được 8,4 (l) CO2, 1,4 (l) N2 (các thể tích đo ở đktc) và 10,125g H2O. Công thức phân tử của X là?
A. C3H7N B. C2H7N C. C3H9N D. C4H9N
Giải: nCO2 = 0,375 mol; nH2O = 0,5625 mol; nN2 = 0,0625 mol
Cách 1: Tìm CTPT dựa vào CTĐGN
nC : nH : nN = nCO2 : 2nH2O : 2nN2 = 0,375 : 0,5625.2 : 0,0625.2 = 3 : 9 : 1
⇒ X có CTPT là (C3H9N)n
Vì X là amin đơn chức nên n = 1 ⇒ Vậy CTPT của X là C3H9N
Cách 2: Thiết lập CTPT:
nAmin = 2.nN2 = 0,125 mol
Số C = nCO2/nAmin = 3; Số H = 2.nH2O/nAmin = 9; Số N = 2.nN2/nAmin = 1
Vậy amin là C3H7N.
Câu 2: Đốt cháy hoàn toàn hỗn hợp 2 amin no, đơn chức, là đồng đẳng liên tiếp, thu được 2,24 lít khí CO2 (đktc) và 3,6 gam H2O. Công thức phân tử của 2 amin là:
A. CH5N và C2H7N B. C2H7N và C3H9N C. C3H9N và C4H11N D. Kết quả khác
Giải: Amin no, đơn chức có CTTQ là CnH2n+3N
Ta có: nCO2 = 0,1 mol; nH2O = 0,2 mol
Ta có:
2 amin đồng đẳng kết tiếp ⇒ 2 amin là CH5N và C2H7N
Cách 2: Với amin no, đơn chức, mạch hở ta có:
Số nguyên tử
Câu 3: Đốt cháy amin A với không khí (N2 và O2 với tỷ lệ mol 4:1) vừa đủ, sau phản ứng thu được 17,6g CO2; 12,6g H2O và 69,44 lít N2 (đktc). Khối lượng của amin là?
A. 9,2g B. 9g C. 11g D. 9,5g
Giải: nCO2 = 0,4 mol; nH2O = 0,7 mol; nN2 = 3,1 mol
Bảo toàn nguyên tố O: 2.nO2 = 2.nCO2 + nH2O ⇒ nO2 = 0,75 mol
Vậy nN2 (kk) = 4.nO2 = 3 mol
⇒ nN2 (pứ cháy) = nN2 – nN2(kk) = 0,1 mol
mAmin = 12.nCO2 + 2.nH2O + 28.nN2 = 9 gam
Câu 4: Đốt cháy hoàn toàn 0,1mol hỗn hợp gồm metylamin, đimetylamin, trimetylamin và etylamin bằng oxi vừa đủ thì thể tích N2 thu được (ở đktc) là
A. 4,48 lít B. 2,24 lít C. 1,12 lít D. 3,36 lít
Giải: Metylamin, đimetylamin; trimetyamin đều là amin đơn chức
⇒ Đặt công thức chung của amin là CxHyN.
⇒ nN2 = 0,5.nAmin = 0,05 mol ⇒

