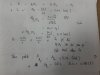[TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
[TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
 Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
Câu 1 : Trình bày cách nhận biết 3 lọ đựng chất bột riêng biệt bị mất nhân, viết phương trình phản ứng xảy ( nếu có) : BaO, P2O5, CaCO3
Câu 2: Cho 2,24 g FE tác dụng với 100 g dung dịch axitsunfuric loãng có nồng độ 24,5 % thu được dung dịch A và khí B.
a, Viết phương trình phản ứng xảy ra.
b, Tính thể tích khí B thu được ở đktc.
c, Tính nộng độ phần trăm của chất có trong dung dịch A.
@bé nương nương @NHOR @Hồng Nhật @Đức Nhật @Tư Âm Diệp Ẩn @Minh Minidora @Minh Dora
Câu 2: Cho 2,24 g FE tác dụng với 100 g dung dịch axitsunfuric loãng có nồng độ 24,5 % thu được dung dịch A và khí B.
a, Viết phương trình phản ứng xảy ra.
b, Tính thể tích khí B thu được ở đktc.
c, Tính nộng độ phần trăm của chất có trong dung dịch A.
@bé nương nương @NHOR @Hồng Nhật @Đức Nhật @Tư Âm Diệp Ẩn @Minh Minidora @Minh Dora