- 25 Tháng mười 2018
- 1,560
- 1,684
- 251
- 29
- Quảng Bình
- Đại học Sư phạm Huế
 [TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
[TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
 Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
1. Định nghĩa
- Khi thay thế nhóm -OH trong phân tử axit bằng gốc -Ỏ thì thu được este.
RCOOH (Axit) → RCOOR’ (Este)
Trong đó: R’ ≠ H
-
Chú ý: Các cách viết khác của este
R – COO – R’ hoặc R’ – OOC – R hoặc R’ – OCO – R (R’ ≠ H)
R là gốc xuất phát từ axit, còn R’ là gốc xuất phát từ ancol.
2. Phân loại
- Este tạo bởi axit đơn chức và ancol đơn chức: RCOOR’.
+ Este tạo bởi axit no đơn chức và ancol no đơn chức:
CnH2n + 1COOCmH2m + 1 hay CxH2xO2 (n ³ 0, m ³ 1, x ³ 2).
- Este tạo bởi axit đơn chức và ancol đa chức: (RCOO)nR’ (n ≥ 2)
- Este tạo bởi axit đa chức và ancol đơn chức: R(COOR’)n (n ≥ 2)
- Este tạo bởi axit đa chức và ancol đa chức: Rn(COO)nmR’m (m ≥ 2; n ≥ 2)
Tóm lại có thể đặt CTPT tổng quát của este: CxHyOz (x, z > 2; y là số chẵn, y ≤ 2x)
3. Danh pháp:
R – COO – R’
Tên gốc hiđcacbon R’ + tên anion gốc axit (đuôi “at”).
VD: HCOOCH3: metyl fomat
C6H5COOC2H5: etyl benzoat
CH3CH2COOCH=CH2: vinyl axetat/vinyl eatnoat
4. Tính chất vật lí

- Trạng thái: Đa số ở trạng thái lỏng. Những este có KLPT rất lớn thể ở trạng thái rắn (như mỡ động vật, sáp ong,…)
- (có cùng số nguyên tử C) vì giữa các phân tử este không có liên kết hiđro.
(có cùng số nguyên tử C) vì giữa các phân tử este không có liên kết hiđro.
- Tính tan: Ít tan hoặc không tan trong nước do không tạo liên kết hidro giữa các phân tử nước.
- Các este thường có mùi thơm đặc trưng:
VD: Isoamyl axetat: mùi chuối; Etyl butirat: mùi dứa; ...
5. Tính chất hóa học
- Phản ứng thủy phân este:
+ Trong môi trường axit: là phản ứng thuận nghịch
RCOOR’ + H – OH ⇌ (H2SO4, to) RCOOH + R’OH
+ Trong môi trường kiềm (phản ứng xà phòng hóa): là phản ứng một chiều
RCOOR’ + NaOH → (to) RCOONa + R’OH
Lưu ý:
+ Nếu nNaOH phản ứng = nEste ⇒ Este đơn chức
Nếu nNaOH = a.nEste (a > 1) ⇒ Este đa chức
+ Nếu RCOOR’ (este đơn chức), trong đó R’ là C6H5- hoặc vòng benzen có nhóm thế ⇒ nNaOH phản ứng = 2nEste và sản phẩm cho 2 muối, trong đó có muối phenolat (C6H5ONa).
+ Khi thủy phân este có cấu tạo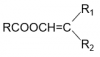
. Nếu R1 hoặc R2 ≠ H ⇒Sản phẩm thủy phân cho xeton.
. Nếu R1 và R2 ≠ H ⇒ Sản phẩm thủy phân cho anđehit.
+ Nếu ở gốc hidrocacbon của R’ một nguyên tử C gắn với nhiều gốc este hoặc có chứa nguyên tử halogen thì khi thủy phân có thể chuyển hóa thành anđehit hoặc xeton hoặc axit cacboxylic.
C2H5COOCHClCH3 + NaOH → C2H5COONa + CH3CHO
+ Este vòng: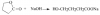
- Phản ứng đốt cháy:
CnH2nO2 + (3n – 2)/2 O2 → (to) nCO2 + nH2O
⇒ Đốt cháy este no, đơn chức, mạch hở: nCO2 = nH2O
- Phản ứng khử:
RCOOR’ → (LiAlH4) RCH2OH + R’OH
- Khi thay thế nhóm -OH trong phân tử axit bằng gốc -Ỏ thì thu được este.
RCOOH (Axit) → RCOOR’ (Este)
Trong đó: R’ ≠ H
-
Chú ý: Các cách viết khác của este
R – COO – R’ hoặc R’ – OOC – R hoặc R’ – OCO – R (R’ ≠ H)
R là gốc xuất phát từ axit, còn R’ là gốc xuất phát từ ancol.
2. Phân loại
- Este tạo bởi axit đơn chức và ancol đơn chức: RCOOR’.
+ Este tạo bởi axit no đơn chức và ancol no đơn chức:
CnH2n + 1COOCmH2m + 1 hay CxH2xO2 (n ³ 0, m ³ 1, x ³ 2).
- Este tạo bởi axit đơn chức và ancol đa chức: (RCOO)nR’ (n ≥ 2)
- Este tạo bởi axit đa chức và ancol đơn chức: R(COOR’)n (n ≥ 2)
- Este tạo bởi axit đa chức và ancol đa chức: Rn(COO)nmR’m (m ≥ 2; n ≥ 2)
Tóm lại có thể đặt CTPT tổng quát của este: CxHyOz (x, z > 2; y là số chẵn, y ≤ 2x)
3. Danh pháp:
R – COO – R’
Tên gốc hiđcacbon R’ + tên anion gốc axit (đuôi “at”).
VD: HCOOCH3: metyl fomat
C6H5COOC2H5: etyl benzoat
CH3CH2COOCH=CH2: vinyl axetat/vinyl eatnoat
4. Tính chất vật lí

- Trạng thái: Đa số ở trạng thái lỏng. Những este có KLPT rất lớn thể ở trạng thái rắn (như mỡ động vật, sáp ong,…)
-
- Tính tan: Ít tan hoặc không tan trong nước do không tạo liên kết hidro giữa các phân tử nước.
- Các este thường có mùi thơm đặc trưng:
VD: Isoamyl axetat: mùi chuối; Etyl butirat: mùi dứa; ...
5. Tính chất hóa học
- Phản ứng thủy phân este:
+ Trong môi trường axit: là phản ứng thuận nghịch
RCOOR’ + H – OH ⇌ (H2SO4, to) RCOOH + R’OH
+ Trong môi trường kiềm (phản ứng xà phòng hóa): là phản ứng một chiều
RCOOR’ + NaOH → (to) RCOONa + R’OH
Lưu ý:
+ Nếu nNaOH phản ứng = nEste ⇒ Este đơn chức
Nếu nNaOH = a.nEste (a > 1) ⇒ Este đa chức
+ Nếu RCOOR’ (este đơn chức), trong đó R’ là C6H5- hoặc vòng benzen có nhóm thế ⇒ nNaOH phản ứng = 2nEste và sản phẩm cho 2 muối, trong đó có muối phenolat (C6H5ONa).
+ Khi thủy phân este có cấu tạo

. Nếu R1 hoặc R2 ≠ H ⇒Sản phẩm thủy phân cho xeton.
. Nếu R1 và R2 ≠ H ⇒ Sản phẩm thủy phân cho anđehit.
+ Nếu ở gốc hidrocacbon của R’ một nguyên tử C gắn với nhiều gốc este hoặc có chứa nguyên tử halogen thì khi thủy phân có thể chuyển hóa thành anđehit hoặc xeton hoặc axit cacboxylic.
C2H5COOCHClCH3 + NaOH → C2H5COONa + CH3CHO
+ Este vòng:
- Phản ứng đốt cháy:
CnH2nO2 + (3n – 2)/2 O2 → (to) nCO2 + nH2O
⇒ Đốt cháy este no, đơn chức, mạch hở: nCO2 = nH2O
- Phản ứng khử:
RCOOR’ → (LiAlH4) RCH2OH + R’OH

