 [TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
[TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
 Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
I,PHẦN TRẮC NGHIỆM
Câu 1: Dãy các chất nào sau đây đều tác dụng với axit clohidric?
A. [imath]Fe_2O_3, KMnO_4, Cu, AgNO_3[/imath].
B. [imath]Fe_2O_3, KMnO_4¸ CuO, AgNO_3[/imath].
C. [imath]Fe, CuO, H_2SO_4, Mg(OH)_2[/imath]
D. [imath]KMnO_4, Cu, H_2SO_4, Mg(OH)_2[/imath].
Câu 2: Kim loại nào sau đây khi tác dụng với [imath]HCl[/imath] và Clo cho cùng một muối clorua kim loại:
A. [imath]Fe[/imath]
B. [imath]Mg[/imath]
C. [imath]Ag[/imath]
D. [imath]Cu[/imath]
Câu 3: cho 15,8 gam [imath]KMnO_4[/imath] tác dụng với dd [imath]HCl[/imath] đậm đặc thu được V lít khí [imath]Cl_2[/imath] (đktc). Giá trị của V
A. 5,6 lít
B. 2,8 lít
C. 0,28
D. 0,56 lít
Câu 4: Tính oxi hóa của các halogen giảm dần theo thứ tự nào sau đây:
A.[imath]I_2 > Br_2 > Cl_2 > F_2[/imath].
B. [imath]Cl_2 > F_2 > Br_2 > I_2[/imath].
C. [imath]F_2 > Cl_2 > Br_2 > I_2[/imath].
D. [imath]Cl_2 > Br_2 > I_2 > F_2[/imath].
Câu 5: [imath]H_2SO_4[/imath] đặc, nguội không phản ứng với các kim loại nào sau đây?
A. [imath]Cu, Fe, Mg[/imath]
B. [imath]Al, Mg, Cu[/imath]
C. [imath]Al, Fe, Cr[/imath]
D. [imath]Fe, Zn, Mg[/imath]
Câu 6: Hơi thuỷ ngân rất độc, bởi vậy khi làm vỡ nhiệt kế thuỷ ngân thì chất bột được dùng để rắc lên thuỷ ngân rồi gom lại là
A. lưu huỳnh.
B. vôi sống.
C. cát.
D. muối ăn.
Câu 7: Để phân biệt dung dịch Natri clorua và dung dịch Natri florua, người ta có thể dùng thuốc thử nào trong các chất sau đây:
A. Dung dịch [imath]AgNO_3[/imath].
B. Dung dịch [imath]Ca(OH)_2[/imath].
C. Dung dịch Flo.
D. Dung dịch [imath]Ba(OH)_2[/imath].
Câu 8: Hoà tan m gam [imath]Fe[/imath] trong dung dịch [imath]HCl[/imath] dư, sau khi phản ứng kết thúc thu được 4,48 lít khí [imath]H_2[/imath] (ở đktc). Giá trị của m là
A. 2,8.
B. 1,4.
C. 5,6.
D. 11,2.
Câu 9:Nguyên tắc pha loãng axit Sunfuric đặc là:
A. Rót từ từ nước vào axit và đun nhẹ
B. Rót từ từ axit vào nước và đun nhẹ
C. Rót từ từ nước vào axit và khuấy nhẹ
D. Rót từ từ axit vào nước và khuấy nhẹ
Câu 10: Dẫn 2,24 lít khí [imath]SO_2[/imath] vào 150 ml dung dịch [imath]NaOH[/imath] 1M, dung dịch thu được có chứa
A. [imath]Na_2SO_3[/imath] và [imath]NaOH[/imath]
B. [imath]Na_2SO_3[/imath]
C. [imath]NaHSO_3[/imath] và [imath]Na_2SO_3[/imath]
D. [imath]NaHSO_3[/imath]
Câu 11: Công thức nào sau đây là của Oleum?
A. [imath]HNO_3.nSO_3[/imath]
B. [imath]H_2SO_3.nSO_3[/imath]
C. [imath]H_2SO_4[/imath]
D. [imath]H_2SO_4.nSO_3[/imath]
Câu 12: Cho các phản ứng sau:
(1) [imath]SO_2 + NaOH → NaHSO_3[/imath] ;
(2) [imath]5SO_2 + 2KMnO_4+ 2H2O → 2H_2SO_4 + K_2SO_4 + 2MnSO_4[/imath] ;
(3) [imath]SO_2 + 2H_2S → 3S + 2H_2O[/imath] ;
(4) [imath]SO_2 + 2H_2O + Br_2 → 2HBr + H_2SO4[/imath] .
Những phản ứng trong đó [imath]SO_2[/imath] thể hiện tính khử là:
A .3.
B. 2 và 4.
C. 3 và 4
D. 1, 2 và 4.
Câu 13:Câu nào sau đây diễn tả đúng tính chất hóa học của lưu huỳnh?
A .Lưu huỳnh chỉ có tính khử.
B. Tất cả đều sai.
C. Lưu huỳnh chỉ có tính oxi hóa.
D. Lưu huỳnh vừa có tính khử, vừa có tính oxi hóa.
Câu 14: Dãy kim loại phản ứng được với [imath]H_2SO_4[/imath] loãng là:
A. [imath]K, Mg, Al[/imath]
B. [imath]Ag, Ba, Fe[/imath]
C. [imath]Zn, Ag, Cu[/imath]
D. [imath]Au, Fe, Na[/imath]
Câu 15: Cho các phát biểu sau:
(a) Tính chất hóa học cơ bản của các halogen là tính oxi hóa mạnh
(b) Khi đi từ flo đến iot, nhiệt độ sôi và nhiệt độ nóng chảy của các đơn chất halogen tăng dần,
(c) Trong hợp chất, halogen có số oxi hóa: -1, +1, +3, +5, +7,
(d) Trong tự nhiên, hoalogen chủ yếu tồn tại ở dạng đơn chất
(e) Ở điều kiện thường, brom lỏng màu đỏ nâu, dễ bay hơi và bị thăng hoa.
Số phát biểu đúng là
A. 3
B. 1
C. 2
D. 4
Câu 16: Trong các thí nghiệm cho kim loại tác dụng với [imath]H_2SO_4[/imath] đặc nóng, sau phản ứng thường sinh ra một lượng lớn khí [imath]SO_2[/imath] ( khí này rất độc, ảnh hưởng đến đường hô hấp..) Vậy để bảo vệ sức khỏe của người làm thí nghiệm ta xử lí khí [imath]SO_2[/imath] bằng:
A. Bông tẩm xút
B. Bông tẩm [imath]KMnO_4[/imath]
C. Bông tẩm muối ăn
D. Cả A và B
Câu 17: Số oxi hóa của [imath]Cl[/imath] trong các chất sau: [imath]NaCl, Cl_2, KClO_3, HClO[/imath] lần lượt là:
A. +1; 0; +3; +1.
B. -1; 0; +5; +1.
C. 0; -1; +3; +2.
D. -1; 0; +1; +5.
Câu 18: Khí oxi có lẫn ít khí clo để thu được khí oxi tinh khiết người ta dẫn hỗn hợp khí qua dung dịch nào sau đây:
A. [imath]NaOH[/imath]
B. [imath]NaC[/imath].
C. [imath]H_2SO_4[/imath] đặc
D. [imath]NaNO_3[/imath]
Câu 19: Hiện tượng đúng khi nhỏ dd [imath]I_2/KI[/imath] vào hồ tinh bột, sau đó đun nóng lên, rồi để nguội là:
A. xuất hiện màu xanh tím, mất màu xanh, màu xanh quay trở lại.
B. xuất hiện màu xanh tím,và màu xanh tím không đổi khi đun nóng hay để nguội.
C. xuất hiện màu đỏ, mất màu đỏ, màu đỏ quay trở lại.
D. xuất hiện màu xanh dương, mất màu xanh, màu xanh quay trở lại.
Câu 20: Cặp thuốc thử dùng để phân biệt 3 dung dịch không màu sau: [imath]NaCl, Na_2SO_4, H_2SO_4[/imath] là:
A. [imath]AgNO_3[/imath], Qùy tím
B. Qùy tím, [imath]BaCl_2[/imath]
C. [imath]NaOH, HCl[/imath]
D. [imath]H_2SO_4, AgNO_3[/imath]
Câu 21: Cho hỗn hợp 6,4 gam [imath]Cu[/imath] và 5,6 gam [imath]Fe[/imath] tác dụng với lượng dư dung dịch axit [imath]H_2SO_4[/imath] đặc nóng, sau phản ứng thu được V lít khí [imath]SO_2[/imath] (đktc) giá trị của V là:
A. 11,2
B. 22,4
C. 5,6
D.6,72
Câu 22: Cho [imath]O[/imath] (Z =8) cấu hình electron của [imath]O^{2-}[/imath] là:
A. [imath]1s^22s^22p^4[/imath]
B. [imath]1s^22s^22p^2[/imath]
C. [imath]1s^22s^22p^6[/imath]
D. [imath]1s^22s^22p^63s^2[/imath]
Câu 23: Nước Gia – ven là hỗn hợp các chất nào sau đây?
A. [imath]HCl, HClO, H_2O[/imath]
B. [imath]NaCl, NaClO, H_2O[/imath]
C. [imath]NaCl, NaClO_3, H_2O[/imath]
D.[imath]NaCl, NaClO_4,H_2O[/imath]
Câu 24: Đây là mô hình điều chế [imath]SO_2[/imath] trong phòng thí nghiệm. quan sát mô hình và cho biết, khí [imath]SO_2[/imath] thu bằng phương pháp nào và tại sao trên bình khí lại có bông tẩm [imath]NaOH[/imath]:
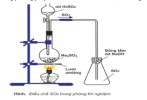
A. Phương pháp đẩy không khí, dùng bông tẩm [imath]NaOH[/imath] ngăn không cho [imath]SO_2[/imath] dư thoát ra ngoài.
B. Phương pháp đẩy nước, dùng bông tẩm [imath]NaOH[/imath] để cho khí tinh khiết hơn.
C. Phương pháp đẩy không khí, dùng bông tẩm [imath]NaOH[/imath] ngăn [imath]O_2[/imath] đi vào bình.
D. Phương pháp đẩy nước, dùng bông tẩm [imath]NaOH[/imath] ngăn không cho [imath]SO_2[/imath] dư thoát ra ngoài
II. PHẦN TỰ LUẬN
Câu 1: (2,0 điểm) Hoàn thành chuỗi phản ứng sau, cân bằng và ghi rõ điều kiện (nếu có).
[imath]S \to SO_2 \to H_2SO_4 \to Fe_2(SO_4)_3 \to BaSO_4[/imath]
Câu 2: (2,0 điểm). Cho 13,6 gam hỗn hợp hai kim loại [imath]Fe[/imath] và [imath]Mg[/imath] tác dụng với dung dịch [imath]H_2SO_4[/imath] loãng dư, thu được 6,72 lit khí [imath]H_2[/imath].
a) Viết các phương trình phản ứng xảy ra.
b) Tính m và thành phần % về khối lượng mỗi kim loại trong hỗn hợp .
c) Cũng khối lượng [imath]Fe[/imath] trên để lâu ngoài không khí , sau một thời gian thu được 14,4 gam hỗn hợp X gồm: [imath]Fe, FeO, Fe_3O_4, Fe_2O_3[/imath]. Cho X phản ứng với lượng dư axit [imath]H_2SO_4[/imath] đặc nóng, thu được V lít [imath]SO_2[/imath] (đktc). Giá trị của V là ?
Câu 1: Dãy các chất nào sau đây đều tác dụng với axit clohidric?
A. [imath]Fe_2O_3, KMnO_4, Cu, AgNO_3[/imath].
B. [imath]Fe_2O_3, KMnO_4¸ CuO, AgNO_3[/imath].
C. [imath]Fe, CuO, H_2SO_4, Mg(OH)_2[/imath]
D. [imath]KMnO_4, Cu, H_2SO_4, Mg(OH)_2[/imath].
Câu 2: Kim loại nào sau đây khi tác dụng với [imath]HCl[/imath] và Clo cho cùng một muối clorua kim loại:
A. [imath]Fe[/imath]
B. [imath]Mg[/imath]
C. [imath]Ag[/imath]
D. [imath]Cu[/imath]
Câu 3: cho 15,8 gam [imath]KMnO_4[/imath] tác dụng với dd [imath]HCl[/imath] đậm đặc thu được V lít khí [imath]Cl_2[/imath] (đktc). Giá trị của V
A. 5,6 lít
B. 2,8 lít
C. 0,28
D. 0,56 lít
Câu 4: Tính oxi hóa của các halogen giảm dần theo thứ tự nào sau đây:
A.[imath]I_2 > Br_2 > Cl_2 > F_2[/imath].
B. [imath]Cl_2 > F_2 > Br_2 > I_2[/imath].
C. [imath]F_2 > Cl_2 > Br_2 > I_2[/imath].
D. [imath]Cl_2 > Br_2 > I_2 > F_2[/imath].
Câu 5: [imath]H_2SO_4[/imath] đặc, nguội không phản ứng với các kim loại nào sau đây?
A. [imath]Cu, Fe, Mg[/imath]
B. [imath]Al, Mg, Cu[/imath]
C. [imath]Al, Fe, Cr[/imath]
D. [imath]Fe, Zn, Mg[/imath]
Câu 6: Hơi thuỷ ngân rất độc, bởi vậy khi làm vỡ nhiệt kế thuỷ ngân thì chất bột được dùng để rắc lên thuỷ ngân rồi gom lại là
A. lưu huỳnh.
B. vôi sống.
C. cát.
D. muối ăn.
Câu 7: Để phân biệt dung dịch Natri clorua và dung dịch Natri florua, người ta có thể dùng thuốc thử nào trong các chất sau đây:
A. Dung dịch [imath]AgNO_3[/imath].
B. Dung dịch [imath]Ca(OH)_2[/imath].
C. Dung dịch Flo.
D. Dung dịch [imath]Ba(OH)_2[/imath].
Câu 8: Hoà tan m gam [imath]Fe[/imath] trong dung dịch [imath]HCl[/imath] dư, sau khi phản ứng kết thúc thu được 4,48 lít khí [imath]H_2[/imath] (ở đktc). Giá trị của m là
A. 2,8.
B. 1,4.
C. 5,6.
D. 11,2.
Câu 9:Nguyên tắc pha loãng axit Sunfuric đặc là:
A. Rót từ từ nước vào axit và đun nhẹ
B. Rót từ từ axit vào nước và đun nhẹ
C. Rót từ từ nước vào axit và khuấy nhẹ
D. Rót từ từ axit vào nước và khuấy nhẹ
Câu 10: Dẫn 2,24 lít khí [imath]SO_2[/imath] vào 150 ml dung dịch [imath]NaOH[/imath] 1M, dung dịch thu được có chứa
A. [imath]Na_2SO_3[/imath] và [imath]NaOH[/imath]
B. [imath]Na_2SO_3[/imath]
C. [imath]NaHSO_3[/imath] và [imath]Na_2SO_3[/imath]
D. [imath]NaHSO_3[/imath]
Câu 11: Công thức nào sau đây là của Oleum?
A. [imath]HNO_3.nSO_3[/imath]
B. [imath]H_2SO_3.nSO_3[/imath]
C. [imath]H_2SO_4[/imath]
D. [imath]H_2SO_4.nSO_3[/imath]
Câu 12: Cho các phản ứng sau:
(1) [imath]SO_2 + NaOH → NaHSO_3[/imath] ;
(2) [imath]5SO_2 + 2KMnO_4+ 2H2O → 2H_2SO_4 + K_2SO_4 + 2MnSO_4[/imath] ;
(3) [imath]SO_2 + 2H_2S → 3S + 2H_2O[/imath] ;
(4) [imath]SO_2 + 2H_2O + Br_2 → 2HBr + H_2SO4[/imath] .
Những phản ứng trong đó [imath]SO_2[/imath] thể hiện tính khử là:
A .3.
B. 2 và 4.
C. 3 và 4
D. 1, 2 và 4.
Câu 13:Câu nào sau đây diễn tả đúng tính chất hóa học của lưu huỳnh?
A .Lưu huỳnh chỉ có tính khử.
B. Tất cả đều sai.
C. Lưu huỳnh chỉ có tính oxi hóa.
D. Lưu huỳnh vừa có tính khử, vừa có tính oxi hóa.
Câu 14: Dãy kim loại phản ứng được với [imath]H_2SO_4[/imath] loãng là:
A. [imath]K, Mg, Al[/imath]
B. [imath]Ag, Ba, Fe[/imath]
C. [imath]Zn, Ag, Cu[/imath]
D. [imath]Au, Fe, Na[/imath]
Câu 15: Cho các phát biểu sau:
(a) Tính chất hóa học cơ bản của các halogen là tính oxi hóa mạnh
(b) Khi đi từ flo đến iot, nhiệt độ sôi và nhiệt độ nóng chảy của các đơn chất halogen tăng dần,
(c) Trong hợp chất, halogen có số oxi hóa: -1, +1, +3, +5, +7,
(d) Trong tự nhiên, hoalogen chủ yếu tồn tại ở dạng đơn chất
(e) Ở điều kiện thường, brom lỏng màu đỏ nâu, dễ bay hơi và bị thăng hoa.
Số phát biểu đúng là
A. 3
B. 1
C. 2
D. 4
Câu 16: Trong các thí nghiệm cho kim loại tác dụng với [imath]H_2SO_4[/imath] đặc nóng, sau phản ứng thường sinh ra một lượng lớn khí [imath]SO_2[/imath] ( khí này rất độc, ảnh hưởng đến đường hô hấp..) Vậy để bảo vệ sức khỏe của người làm thí nghiệm ta xử lí khí [imath]SO_2[/imath] bằng:
A. Bông tẩm xút
B. Bông tẩm [imath]KMnO_4[/imath]
C. Bông tẩm muối ăn
D. Cả A và B
Câu 17: Số oxi hóa của [imath]Cl[/imath] trong các chất sau: [imath]NaCl, Cl_2, KClO_3, HClO[/imath] lần lượt là:
A. +1; 0; +3; +1.
B. -1; 0; +5; +1.
C. 0; -1; +3; +2.
D. -1; 0; +1; +5.
Câu 18: Khí oxi có lẫn ít khí clo để thu được khí oxi tinh khiết người ta dẫn hỗn hợp khí qua dung dịch nào sau đây:
A. [imath]NaOH[/imath]
B. [imath]NaC[/imath].
C. [imath]H_2SO_4[/imath] đặc
D. [imath]NaNO_3[/imath]
Câu 19: Hiện tượng đúng khi nhỏ dd [imath]I_2/KI[/imath] vào hồ tinh bột, sau đó đun nóng lên, rồi để nguội là:
A. xuất hiện màu xanh tím, mất màu xanh, màu xanh quay trở lại.
B. xuất hiện màu xanh tím,và màu xanh tím không đổi khi đun nóng hay để nguội.
C. xuất hiện màu đỏ, mất màu đỏ, màu đỏ quay trở lại.
D. xuất hiện màu xanh dương, mất màu xanh, màu xanh quay trở lại.
Câu 20: Cặp thuốc thử dùng để phân biệt 3 dung dịch không màu sau: [imath]NaCl, Na_2SO_4, H_2SO_4[/imath] là:
A. [imath]AgNO_3[/imath], Qùy tím
B. Qùy tím, [imath]BaCl_2[/imath]
C. [imath]NaOH, HCl[/imath]
D. [imath]H_2SO_4, AgNO_3[/imath]
Câu 21: Cho hỗn hợp 6,4 gam [imath]Cu[/imath] và 5,6 gam [imath]Fe[/imath] tác dụng với lượng dư dung dịch axit [imath]H_2SO_4[/imath] đặc nóng, sau phản ứng thu được V lít khí [imath]SO_2[/imath] (đktc) giá trị của V là:
A. 11,2
B. 22,4
C. 5,6
D.6,72
Câu 22: Cho [imath]O[/imath] (Z =8) cấu hình electron của [imath]O^{2-}[/imath] là:
A. [imath]1s^22s^22p^4[/imath]
B. [imath]1s^22s^22p^2[/imath]
C. [imath]1s^22s^22p^6[/imath]
D. [imath]1s^22s^22p^63s^2[/imath]
Câu 23: Nước Gia – ven là hỗn hợp các chất nào sau đây?
A. [imath]HCl, HClO, H_2O[/imath]
B. [imath]NaCl, NaClO, H_2O[/imath]
C. [imath]NaCl, NaClO_3, H_2O[/imath]
D.[imath]NaCl, NaClO_4,H_2O[/imath]
Câu 24: Đây là mô hình điều chế [imath]SO_2[/imath] trong phòng thí nghiệm. quan sát mô hình và cho biết, khí [imath]SO_2[/imath] thu bằng phương pháp nào và tại sao trên bình khí lại có bông tẩm [imath]NaOH[/imath]:

A. Phương pháp đẩy không khí, dùng bông tẩm [imath]NaOH[/imath] ngăn không cho [imath]SO_2[/imath] dư thoát ra ngoài.
B. Phương pháp đẩy nước, dùng bông tẩm [imath]NaOH[/imath] để cho khí tinh khiết hơn.
C. Phương pháp đẩy không khí, dùng bông tẩm [imath]NaOH[/imath] ngăn [imath]O_2[/imath] đi vào bình.
D. Phương pháp đẩy nước, dùng bông tẩm [imath]NaOH[/imath] ngăn không cho [imath]SO_2[/imath] dư thoát ra ngoài
II. PHẦN TỰ LUẬN
Câu 1: (2,0 điểm) Hoàn thành chuỗi phản ứng sau, cân bằng và ghi rõ điều kiện (nếu có).
[imath]S \to SO_2 \to H_2SO_4 \to Fe_2(SO_4)_3 \to BaSO_4[/imath]
Câu 2: (2,0 điểm). Cho 13,6 gam hỗn hợp hai kim loại [imath]Fe[/imath] và [imath]Mg[/imath] tác dụng với dung dịch [imath]H_2SO_4[/imath] loãng dư, thu được 6,72 lit khí [imath]H_2[/imath].
a) Viết các phương trình phản ứng xảy ra.
b) Tính m và thành phần % về khối lượng mỗi kim loại trong hỗn hợp .
c) Cũng khối lượng [imath]Fe[/imath] trên để lâu ngoài không khí , sau một thời gian thu được 14,4 gam hỗn hợp X gồm: [imath]Fe, FeO, Fe_3O_4, Fe_2O_3[/imath]. Cho X phản ứng với lượng dư axit [imath]H_2SO_4[/imath] đặc nóng, thu được V lít [imath]SO_2[/imath] (đktc). Giá trị của V là ?

