- 26 Tháng tám 2021
- 1,369
- 1,660
- 216
- Bình Định
- Viện dầu và cây có dầu
 [TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
[TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
 Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
AMIN
I. Khái niệm, phân loại
1. Khái niệm
- Khi thay thế một hay nhiều nguyên tử hiđro trong phân tử NH3 bằng một hay nhiều gốc hiđrocacbon ta được amin.
Ví dụ:
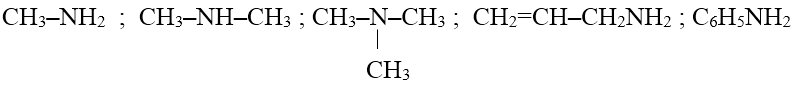
2. Phân loại
a. Theo gốc hiđrocacbon:
– Amin không thơm: $CH_3NH_2$, $C_2H_5NH_2$, ...
– Amin thơm: $C_6H_5NH_2$, $CH_3C_6H_4NH_2$, ...
– Amin dị vòng:
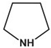
b. Theo bậc amin: là số nguyên tử H trong phân tử NH3 bị thay thế bởi gốc hiđrocacbon. Theo đó, các amin được phân loại thành:
| Amin bậc I | Amin bậc II | Amin bậc III |
|---|---|---|
| R–NH2 | R–NH–R’ |
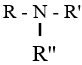
|
| R, R’ và R’’ là gốc hiđrocacbon | � |
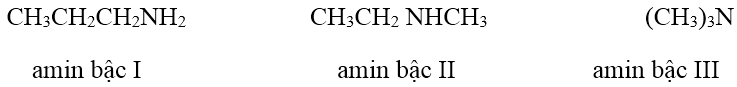
1. Đồng phân
– Đồng phân về mạch cacbon.
– Đồng phân vị trí nhóm chức.
– Đồng phân về bậc của amin.
Ví dụ: Các đồng phân của $C_4H_{11}N$.
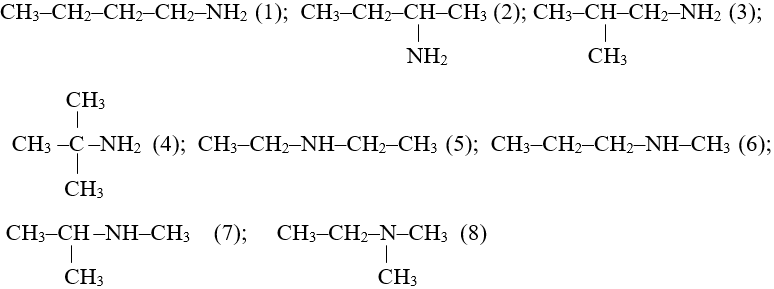
2. Danh pháp
a. Cách gọi tên theo danh pháp gốc – chức: Tên gốc hiđrocacbon + amin
Ví dụ: $CH_3NH_2$ (Metylamin), $C_2H_5–NH_2$ (Etylamin), $CH_3CH(NH_2)CH_3$ (Isopropylamin), …
b. Cách gọi tên theo danh pháp thay thế: Tên hiđrocacbon + vị trí + amin
Ví dụ: $CH_3NH_2$ (Metanamin), $C_2H_5–NH_2$ (Etanamin), $CH_3CH(NH_2)CH_3$ (Propan - 2 - amin), ...
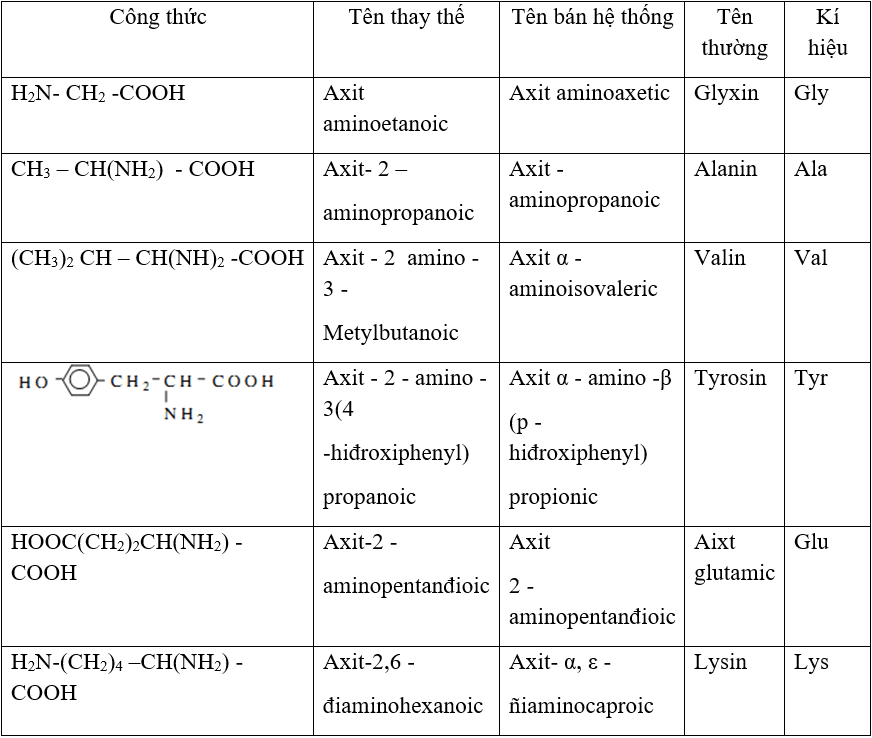
c. Tên thông thường chỉ áp dụng với một số amin:
Tên gọi của một số amin
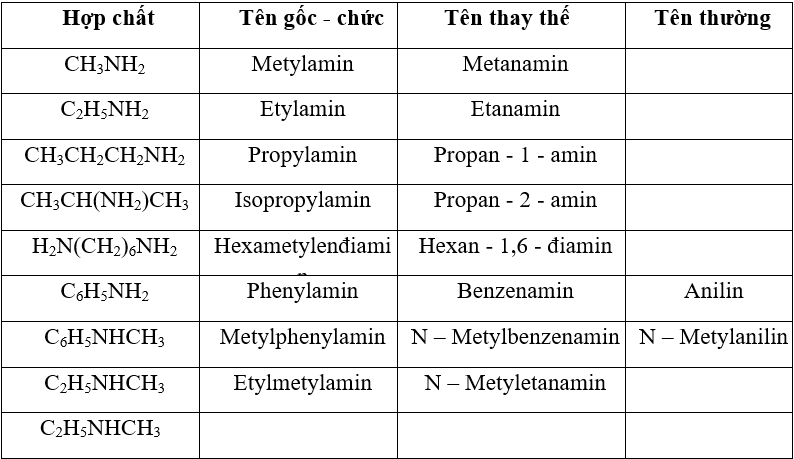
- Lưu ý:
– Tên các nhóm ankyl đọc theo thứ tự chữ cái a, b, c, … + amin.
– Với các amin bậc 2 và 3, chọn mạch dài nhất chứa N làm mạch chính:
+ Có 2 nhóm ankyl → thêm 1 chữ N ở đầu.
Ví dụ: $CH_3–NH–C_2H_5$: N–etyl metyl amin.
+ Có 3 nhóm ankyl → thêm 2 chữ N ở đầu (nếu trong 3 nhóm thế có 2 nhóm giống nhau).
Ví dụ: $CH_3–N(CH_3)–C_2H_5$: N, N–etyl đimetyl amin.
+ Có 3 nhóm ankyl khác nhau → 2 chữ N cách nhau 1 tên ankyl.
Ví dụ: $CH_3–N(C_2H_5)–C_3H_7$: N–etyl–N–metyl propyl amin.
– Khi nhóm –NH2 đóng vai trò nhóm thế thì gọi là nhóm amino.
Ví dụ: $CH_3CH(NH_2)COOH$ (axit 2–aminopropanoic).
III. Tính chất vật lý
- Chất rắn, dạng tinh thể, không màu, vị hơi ngọt.
- Nhiệt độ nóng chảy cao, dễ tan trong nước vì amino axit tồn tại ở dạng ion lưỡng cực:

- Anilin là chất lỏng, nhiệt độ sôi là 184oC, không màu, rất độc, ít tan trong nước, tan trong ancol và benzen.
IV. Cấu tạo phân tử và tính chất hóa học
1. Cấu tạo phân tử
- Trong phân tử amin đều có nguyên tử nitơ còn một cặp electron tự do chưa liên kết có thể tạo cho – nhận giống NH3.
⇒ Vì vậy các amin có tính bazơ giống $NH_3$ (tức tính bazơ của amin = tính bazơ của NH3).
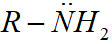
a. Tính bazơ
Do nguyên tử N trong phân tử amin còn cặp e chưa sử dụng có khả năng nhận proton.
* So sánh tính bazơ của các amin:
+ Nếu nguyên tử N trong phân tử amin được gắn với gốc đẩy e (gốc no: ankyl) thì tính bazơ của amin mạnh hơn so với tính bazơ của NH3. Những amin này làm cho quỳ tím chuyển thành màu xanh.
+ Nếu nguyên tử N trong phân tử amin gắn với các gốc hút e (gốc không no, gốc thơm) thì tính bazơ của amin yếu hơn so với tính bazơ của NH3. Những amin này không làm xanh quỳ tím.
+ Amin có càng nhiều gốc đẩy e thì tính bazơ càng mạnh, amin có càng nhiều gốc hút e thì tính bazơ càng yếu.
⇒ Lực bazơ: CnH2n + 1–NH2 > H–NH2 > $C_6H_5–NH_2$
- Dung dịch metylamin và nhiều đồng đẳng của nó có khả năng làm xanh giấy quỳ tím hoặc làm hồng phenolphtalein.
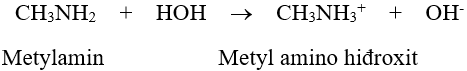
- Anilin và các amin thơm rất ít tan trong nước. Dung dịch của chúng không làm đổ màu quỳ tím và phenolphtalein.
- Tác dụng với axit: R–NH2 + HCl → R–NH3Cl
Ví dụ:
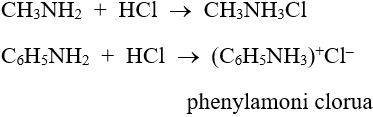
Ví dụ: 3$CH_3NH_2$ + $FeCl_3$ + 3$H_2O$ → $Fe(OH)_3$↓ + 3$CH_3NH_3Cl$
- Lưu ý: Khi cho muối của $Cu^{2+}$, $Zn^{2+}$, … vào dung dịch amin (dư) → hiđroxit kết tủa → kết tủa tan (tạo phức chất).
b. Phản ứng với axit nitrơ $HNO_2$
- Amin bậc một tác dụng với axit nitrơ ở nhiệt độ thường cho ancol hoặc phenol và giải phóng nitơ.
$C_2H_5NH_2$ + HONO → $C_2H_5OH$ + $N_2$↑ + $H_2O$
- Anilin và các amin thơm bậc một tác dụng với axit nitrơ ở nhiệt độ thấp (0 - $5^{C}$) cho muối điazoni:
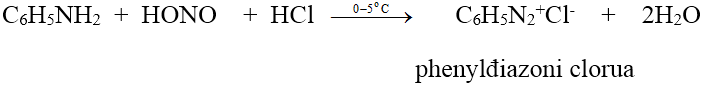
c. Phản ứng ankyl hóa
Amin bậc một hoặc bậc hai tác dụng với ankyl halogenua ($CH_3I$, …) , nguyên tử H của nhóm amin có thể bị thay thế bởi gốc ankyl:
Ví dụ: $C_2H_5NH_2$ + $CH_3I$ → $C_2H_5NHCH_3$ + HI
– Phản ứng này dùng để điều chế amin bậc cao từ amin bậc thấp hơn.
d. Phản ứng thế ở nhân thơm của anilin
Do ảnh hưởng của nhóm $NH_2$ (tương tự nhóm –OH ở phenol), ba nguyên tử H ở các vị trí ortho và para so với nhóm –$NH_2$ trong nhân thơm của anilin bị thay thế bởi ba nguyên tử brom:
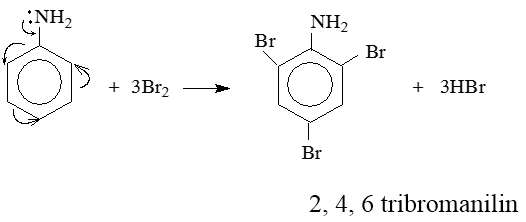
e) Phản ứng cháy của amin no đơn chức mạch hở:
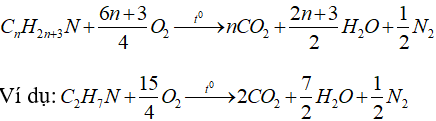
1. Ứng dụng
Các ankylamin được dùng trong tổng hợp hữu cơ, đặc biệt là các điamin được dùng để tổng hợp polime.
Anilin là nguyên liệu quan trọng trong công nghiệp phẩm nhuộm (phẩm azo, đen anilin,...), polime (nhựa anilin - fomanđehit,...), dược phẩm (streptoxit, suafaguaniđin,...)
2. Điều chế
- Thay thế nguyên tử H của phân tử amoniac
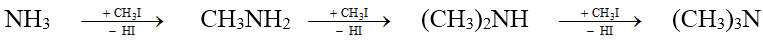
- Khử hợp chất nitro
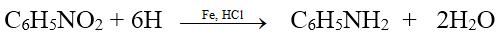
Last edited: