 [TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
[TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
 Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
CHƯƠNG 4: PHẢN ỨNG OXI HÓA KHỬ
A – GIẢI TOÁN BẰNG ĐỊNH LUẬT BẢO TOÀN ELETRON
1. Nguyên tắc
- Tổng số mol e nhường = tổng số mol e nhận (1)
- Định luật bảo toàn e có thể được áp dụng cho các phản ứng riêng hoặc tổng hợp nhiều phản ứng.
2. Cách giải cơ bản với bài toán có vận dụng định luật bảo toàn electron
- Xác định chất khử và chất oxi hoá.
- Viết các quá trình khử và quá trình oxi hoá.
- Sử dụng biểu thức của định luật bảo toàn electron: ne nhường = ne nhận để giải.
BÀI TẬP MẪU
VD1: Cho m(g) Al vào 100ml dung dịch Cu(NO3)2 2M và AgNO3 2M thu được dung dịch A và chất rắn B. Nếu cho B phản ứng với dung dịch HCl dư thì được 3,36 lit H2 (đktc). Tìm m?
Giải
- Nhận thấy trong bài toán trên, Al đóng vai trò chất khử; Ag+, H+ và Cu2+ đóng vai trò chất oxi hóa.
- Các quá trình nhường và nhận e đã xảy ra:
Al → Al3+ + 3e
Ag+ + 1e → Ag
Cu2+ + 2e → Cu
H+ + 1e → 1/2H2
Vận dụng định luật bảo toàn e cho các quá trình trên ta thấy:
3m/27 = 0,1.2.2 + 0,1.2.1 + 3,36.2/22,4 → m = 9(g).
VD2: Để m(g) Fe ngoài không khí, sau một thời gian thu được 12g hỗn hợp gồm 4 chất rắn. Hòa tan hoàn toàn hỗn hợp bằng HNO3 thu được dung dịch A và 2,24 lít NO (đktc). Tìm m
Giải
- Nhận thấy trong bài toán này, Sắt từ mức oxi hóa là 0 được chuyển lên các mức oxi hóa trung gian rồi cuối cùng đạt mức oxi hóa cao nhất là +3 đóng vai trò chất khử. Có 2 chất oxi hóa là O2 và HNO3.
- Các quá trình nhường và nhận e trong bài:
Fe → Fe3+ + 3e
O2 + 4e → 2O-2
N+5 + 3e → N+2 (NO)
Vận dụng định luật bảo toàn e cho các quá trình ta được:
3m/56 = (12 – m).4/32 + 2,24.3/22,4 → m = 10,08
B – LÝ THUYẾT VỀ PHẢN ỨNG OXI HÓA KHỬ
I. KHÁI NIỆM
1. Phản ứng oxi hoá - khử
- Khái niệm: Phản ứng oxi hóa - khử là phản ứng hoá học trong đó có sự chuyển e giữa các chất phản ứng.
- Dấu hiệu nhận biết: Phản ứng có sự thay đổi số oxi hóa của một số nguyên tố.
2. Chất khử (chất bị oxi hoá)
- Khái niệm: Chất khử là chất có khả năng nhường e (cho e).
- Dấu hiệu nhận biêt:
+ Sau phản ứng, số oxi hoá của chất khử tăng.
+ Chất khử có chứa nguyên tố chưa đạt đến mức oxi hoá cao nhất.
Chú ý: Nguyên tố ở nhóm XA có số oxi hoá cao nhất là +X.
3. Chất oxi hoá (chất bị khử)
- Khái niệm: Chất oxi hoá là chất có khả năng nhận e (thu e).
- Dấu hiệu:
+ Sau phản ứng, số oxi hoá của chất oxi hoá giảm.
+ Chất oxi hoá có chứa nguyên tố có mức oxi hoá chưa phải thấp nhất.
Chú ý: Kim loại có số oxi hoá thấp nhất là 0, phi kim thuộc nhóm xA thì số oxi hoá thấp nhất là (x - 8).
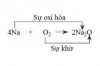
4. Sự khử và sự oxi hoá
- Sự khử (quá trình khử) của một chất là làm cho chất đó nhận electron hay làm giảm số oxi hoá của chất đó.
- Sự oxi hoá (quá trình oxi hoá) của một chất là làm cho chất đó nhường electron hay làm tăng số oxi hoá của chất đó.
II. ĐIỀU KIỆN CỦA PHẢN ỨNG OXI HOÁ - KHỬ
Phải có sự tham gia đồng thời của chất khử và chất oxi hóa. Chất khử và chất oxi hóa phải đủ mạnh.
III. PHÂN LOẠI PHẢN ỨNG OXI HOÁ - KHỬ
Phản ứng oxi hoá - khử được chia thành nhiều loại khác nhau:
- Phản ứng oxi hóa - khử thông thường: chất khử và chất oxi hóa ở 2 phân tử chất khác nhau.
C + 4HNO3 đặc → CO2 + 4NO2 + 2H2O
Cu + 2H2SO4 đặc → CuSO4 + SO2 + 2H2O
- Phản ứng oxi hóa - khử nội phân tử: chất khử và chất oxi hóa thuộc cùng 1 phân tử nhưng ở 2 nguyên tử khác nhau (thường gặp là phản ứng nhiệt phân).
AgNO3 → Ag + NO2 + 1/2O2
Cu(NO3)2 → CuO + 2NO2 + 1/2O2
- Phản ứng tự oxi hóa - khử, chất khử đồng thời cũng là chất oxi hóa (chất khử và chất oxi hoá thuộc về cùng một nguyên tố trong một phân tử chất).
Cl2 + 2NaOH → NaCl + NaClO + H2O
2NO2 + 2NaOH → NaNO2 + NaNO3 + H2O
4KClO3 → 3KClO4 + KCl
C – PHƯƠNG PHÁP THĂNG BẰNG ELECTRON
1. Nguyên tắc
Trong phản ứng oxi hoá - khử luôn tồn tại đồng thời chất oxi hoá (chất nhận e) và chất khử (chất nhường e). Số e mà chất khử nhường luôn bằng số e mà chất oxi hoá nhận.
2. Các bước cân bằng phản ứng oxi hoá - khử theo phương pháp thăng bằng electron
- Xác định số oxi hoá của những nguyên tố thay đổi số oxi hoá.
- Viết quá trình oxi hoá và quá trình khử, cân bằng mỗi quá trình:
+ Dấu "+e" đặt bên có số oxi hoá lớn.
+ Số e = số oxi hoá lớn - số oxi hoá bé.
+ Nhân cả quá trình với chỉ số của nguyên tố thay đổi số oxi hoá nếu chỉ số khác 1 (với các đơn chất có thể chấp nhận giữ nguyên chỉ số).
- Tìm hệ số thích hợp sao cho tổng số e cho bằng tổng số e nhận:
+ Tìm bội chung nhỏ nhất của số e nhường và nhận.
+ Lấy bội chung nhỏ nhất chia cho số e ở từng quá trình được hệ số.
- Đặt hệ số của chất oxi hoá và chất khử vào sơ đồ phản ứng và kiểm tra lại.
A – GIẢI TOÁN BẰNG ĐỊNH LUẬT BẢO TOÀN ELETRON
1. Nguyên tắc
- Tổng số mol e nhường = tổng số mol e nhận (1)
- Định luật bảo toàn e có thể được áp dụng cho các phản ứng riêng hoặc tổng hợp nhiều phản ứng.
2. Cách giải cơ bản với bài toán có vận dụng định luật bảo toàn electron
- Xác định chất khử và chất oxi hoá.
- Viết các quá trình khử và quá trình oxi hoá.
- Sử dụng biểu thức của định luật bảo toàn electron: ne nhường = ne nhận để giải.
BÀI TẬP MẪU
VD1: Cho m(g) Al vào 100ml dung dịch Cu(NO3)2 2M và AgNO3 2M thu được dung dịch A và chất rắn B. Nếu cho B phản ứng với dung dịch HCl dư thì được 3,36 lit H2 (đktc). Tìm m?
Giải
- Nhận thấy trong bài toán trên, Al đóng vai trò chất khử; Ag+, H+ và Cu2+ đóng vai trò chất oxi hóa.
- Các quá trình nhường và nhận e đã xảy ra:
Al → Al3+ + 3e
Ag+ + 1e → Ag
Cu2+ + 2e → Cu
H+ + 1e → 1/2H2
Vận dụng định luật bảo toàn e cho các quá trình trên ta thấy:
3m/27 = 0,1.2.2 + 0,1.2.1 + 3,36.2/22,4 → m = 9(g).
VD2: Để m(g) Fe ngoài không khí, sau một thời gian thu được 12g hỗn hợp gồm 4 chất rắn. Hòa tan hoàn toàn hỗn hợp bằng HNO3 thu được dung dịch A và 2,24 lít NO (đktc). Tìm m
Giải
- Nhận thấy trong bài toán này, Sắt từ mức oxi hóa là 0 được chuyển lên các mức oxi hóa trung gian rồi cuối cùng đạt mức oxi hóa cao nhất là +3 đóng vai trò chất khử. Có 2 chất oxi hóa là O2 và HNO3.
- Các quá trình nhường và nhận e trong bài:
Fe → Fe3+ + 3e
O2 + 4e → 2O-2
N+5 + 3e → N+2 (NO)
Vận dụng định luật bảo toàn e cho các quá trình ta được:
3m/56 = (12 – m).4/32 + 2,24.3/22,4 → m = 10,08
B – LÝ THUYẾT VỀ PHẢN ỨNG OXI HÓA KHỬ
I. KHÁI NIỆM
1. Phản ứng oxi hoá - khử
- Khái niệm: Phản ứng oxi hóa - khử là phản ứng hoá học trong đó có sự chuyển e giữa các chất phản ứng.
- Dấu hiệu nhận biết: Phản ứng có sự thay đổi số oxi hóa của một số nguyên tố.
2. Chất khử (chất bị oxi hoá)
- Khái niệm: Chất khử là chất có khả năng nhường e (cho e).
- Dấu hiệu nhận biêt:
+ Sau phản ứng, số oxi hoá của chất khử tăng.
+ Chất khử có chứa nguyên tố chưa đạt đến mức oxi hoá cao nhất.
Chú ý: Nguyên tố ở nhóm XA có số oxi hoá cao nhất là +X.
3. Chất oxi hoá (chất bị khử)
- Khái niệm: Chất oxi hoá là chất có khả năng nhận e (thu e).
- Dấu hiệu:
+ Sau phản ứng, số oxi hoá của chất oxi hoá giảm.
+ Chất oxi hoá có chứa nguyên tố có mức oxi hoá chưa phải thấp nhất.
Chú ý: Kim loại có số oxi hoá thấp nhất là 0, phi kim thuộc nhóm xA thì số oxi hoá thấp nhất là (x - 8).
4. Sự khử và sự oxi hoá
- Sự khử (quá trình khử) của một chất là làm cho chất đó nhận electron hay làm giảm số oxi hoá của chất đó.
- Sự oxi hoá (quá trình oxi hoá) của một chất là làm cho chất đó nhường electron hay làm tăng số oxi hoá của chất đó.

II. ĐIỀU KIỆN CỦA PHẢN ỨNG OXI HOÁ - KHỬ
Phải có sự tham gia đồng thời của chất khử và chất oxi hóa. Chất khử và chất oxi hóa phải đủ mạnh.
III. PHÂN LOẠI PHẢN ỨNG OXI HOÁ - KHỬ
Phản ứng oxi hoá - khử được chia thành nhiều loại khác nhau:
- Phản ứng oxi hóa - khử thông thường: chất khử và chất oxi hóa ở 2 phân tử chất khác nhau.
C + 4HNO3 đặc → CO2 + 4NO2 + 2H2O
Cu + 2H2SO4 đặc → CuSO4 + SO2 + 2H2O
- Phản ứng oxi hóa - khử nội phân tử: chất khử và chất oxi hóa thuộc cùng 1 phân tử nhưng ở 2 nguyên tử khác nhau (thường gặp là phản ứng nhiệt phân).
AgNO3 → Ag + NO2 + 1/2O2
Cu(NO3)2 → CuO + 2NO2 + 1/2O2
- Phản ứng tự oxi hóa - khử, chất khử đồng thời cũng là chất oxi hóa (chất khử và chất oxi hoá thuộc về cùng một nguyên tố trong một phân tử chất).
Cl2 + 2NaOH → NaCl + NaClO + H2O
2NO2 + 2NaOH → NaNO2 + NaNO3 + H2O
4KClO3 → 3KClO4 + KCl
C – PHƯƠNG PHÁP THĂNG BẰNG ELECTRON
1. Nguyên tắc
Trong phản ứng oxi hoá - khử luôn tồn tại đồng thời chất oxi hoá (chất nhận e) và chất khử (chất nhường e). Số e mà chất khử nhường luôn bằng số e mà chất oxi hoá nhận.
2. Các bước cân bằng phản ứng oxi hoá - khử theo phương pháp thăng bằng electron
- Xác định số oxi hoá của những nguyên tố thay đổi số oxi hoá.
- Viết quá trình oxi hoá và quá trình khử, cân bằng mỗi quá trình:
+ Dấu "+e" đặt bên có số oxi hoá lớn.
+ Số e = số oxi hoá lớn - số oxi hoá bé.
+ Nhân cả quá trình với chỉ số của nguyên tố thay đổi số oxi hoá nếu chỉ số khác 1 (với các đơn chất có thể chấp nhận giữ nguyên chỉ số).
- Tìm hệ số thích hợp sao cho tổng số e cho bằng tổng số e nhận:
+ Tìm bội chung nhỏ nhất của số e nhường và nhận.
+ Lấy bội chung nhỏ nhất chia cho số e ở từng quá trình được hệ số.
- Đặt hệ số của chất oxi hoá và chất khử vào sơ đồ phản ứng và kiểm tra lại.

