- 25 Tháng mười 2018
- 1,560
- 1,684
- 251
- 29
- Quảng Bình
- Đại học Sư phạm Huế
 [TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
[TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
 Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
ĐỘ TAN
1. Khái niệm
Độ tan của một chất trong nước là số gam chất đó tan được trong 100 g nước để tạo thành dung dịch bão hòa ở một nhiệt độ xác định.
⇒ Công thức tính độ tan: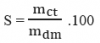
2. Một số công thức liên hệ
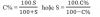
3. Các dạng bài tập về độ tan
Dạng 1: Bài toán liên quan giữa độ tan của một chất và nồng độ phần trăm dung dịch bão hòa của chất đó.
Bài 1: Tính nồng độ % của dung dịch NaCl bão hòa ở 25oC. Biết ở 25oC, độ tan của NaCl là 36.
Ta có: C% = 100S/(100+S) = 26,47%
Bài 2: Tính độ tan của Na2SO4 ở 10oC và nồng độ phần trăm của dung dịch bão hòa Na2SO4 ở nhiệt độ này. Biết rằng ở 10oC khi hòa tan 7,2 gam Na2SO4 vào 80 gam nước thì thu được dung dịch bão hòa Na2SO4.
Giải:
Độ tan của Na2SO4 ở 10oC là: S = mct.100/mdm = 7,2.100/80 = 9
Nồng độ %: C% = 100S/(100 + S) = 7,2/(7,2 + 80) = 8,257%
Dạng 2: Tính lượng tinh thể ngậm nước cần thêm vào dung dịch
Cách làm: Dùng định luật bảo toàn khối lượng để tính:
- mdung dịch tạo thành = mtinh thể + mdung dịch ban đầu
- Khối lượng chất tan trong dung dịch tạo thành
m = mchất tan trong tinh thể + mchất tan trong dung dịch ban đầu.
Với những dạng toán tính lượng tinh thể ngậm nước này, đề bài thường cho sẵn loại tinh thể cần lấy và dung dịch cho sẵn có chứa cùng loại chất tan.
Bài 1: Tính lượng tinh thể CuSO4.5H2O cần lấy để pha chế 500 ml dung dịch CuSO4 8% (D = 1,1 g/ml).
Giải: Khối lượng CuSO4 có trong 500 ml CuSO4 8% là:
mCuSO4 = 500.1,1.8/100 = 44 gam ⇒ nCuSO4 = 0,275 mol
Vậy nCuSO4.5H2O = 0,275 mol
Khối lượng tinh thể CuSO4.5H2O là: m = 250.0,275 = 68,75 gam
Bài 2: Ở 25oC, có 175 gam dung dịch CuSO4 bão hòa. Đung nóng dung dịch lên 90oC, hỏi phải thêm vào dung dịch bao nhiêu gam CuSO4.5H2O để thu được dung dịch bão hòa ở nhiệt độ này. Biết độ tan của CuSO4 khan ở 25oC là 40 và ở 90oC là 80.
Giải:
Ở 25oC, mCuSO4 trong 175gam dung dịch là 40.175/140 = 50 gam
nH2O = 175 – 50 = 125 gam
Đặt a là khối lượng CuSO4.5H2O cần thêm vào:
Trong a gam CuSO4.5H2O có 160a/250 = 0,64a gam CuSO4 và 0,36 gam H2O
Vậy ở 90oC, sau khi thêm CuSO4.5H2O vào 175 gam dung dịch ta có:
mH2O = 125 + 0,36a
mCuSO4 = 50 + 0,64a
Ở 90oC: S = mCuSO4/mH2O = (50 + 0,64a)/(125 + 0,36a) = 80
⇒ a = 142 gam
Vận dụng: Để điều chế 560 gam dung dịch CuSO4 16% cần phải lấy bao nhiêu gam dung dịch CuSO4 8% và bao nhiêu gam tinh thể CuSO4.5H2O.
Dạng 3: Bài toán tính lượng chất tan tách ra hay thêm vào khi thay đổi một nhiệt độ dung dịch bão hòa cho sẵn.
Bài 1: Có 600 gam dung dịch NaCl bão hòa ở 90oC được làm lạnh xuống 0oC. Tính khối lượng kết tinh thu được biết độ tan của NaCl ở 90oC là 50, ở 0oC là 35.
Giải:
Ở 90oC, trong 600 gam dung dịch NaCl bão hòa có: 600.50/150 = 200 gam NaCl.
⇒ mH2O = 600 – 200 = 400 gam
Ở 0oC, trong 400 gam nước có: 400.35/135 = 140 gam
Vậy khối lượng muối NaCl tách ra khỏi dung dịch là 200 – 140 = 60 gam.
Bài 2: Lấy 1000 gam dung dịch Al2(SO4)3 bão hòa làm bay hơi 100 gam H2O. Phần dung dịch còn lại đưa về 10oC thấy có a gam Al2(SO4)3.18H2O kết tinh. Tính a. Biết độ tan của Al2(SO4)3 ở 10oC là 33,5.
Giải:
Xét trong 1000 gam dung dịch Al2(SO4)3 có 250,936 gam Al2(SO4)3 và 749,064 gam H2O
Trong a gam Al2(SO4)3.18H2O có 19a/37 gam Al2(SO4)3 và 18a/37 gam H2O.
Vậy sau khi kết tinh tách ra, dung dịch còn lại có chứa:
mct = 250,936 – 19a/37 (gam)
mH2O = 749,064 – 100 – 18a/37
Độ tan của Al2(SO4)3 ở 10oC là 33,5 nên ta có:
S = mct.100/mH2O = 95,565 gam
Vận dụng:
Bài 1: Giả thiết độ tan của CuSO4 ở 10oC và 80oC lần lượt là 17,4 và 55. Làm lạnh 1500 g dung dịch CuSO4 bão hòa ở 80oC xuống 10oC. Tính số gam CuSO4.5H2O tách ra khỏi dung dịch sau khi làm lạnh.
Bài 2: Xác định độ tan của Na2CO3 trong nước ở 18oC. Biết rằng ở nhiệt độ này, khi hòa tan hết 143 gam muối ngậm nước Na2CO3.10H2O trong 160 gam H2O thì thu được dung dịch bão hòa.
1. Khái niệm
Độ tan của một chất trong nước là số gam chất đó tan được trong 100 g nước để tạo thành dung dịch bão hòa ở một nhiệt độ xác định.
⇒ Công thức tính độ tan:
2. Một số công thức liên hệ
3. Các dạng bài tập về độ tan
Dạng 1: Bài toán liên quan giữa độ tan của một chất và nồng độ phần trăm dung dịch bão hòa của chất đó.
Bài 1: Tính nồng độ % của dung dịch NaCl bão hòa ở 25oC. Biết ở 25oC, độ tan của NaCl là 36.
Ta có: C% = 100S/(100+S) = 26,47%
Bài 2: Tính độ tan của Na2SO4 ở 10oC và nồng độ phần trăm của dung dịch bão hòa Na2SO4 ở nhiệt độ này. Biết rằng ở 10oC khi hòa tan 7,2 gam Na2SO4 vào 80 gam nước thì thu được dung dịch bão hòa Na2SO4.
Giải:
Độ tan của Na2SO4 ở 10oC là: S = mct.100/mdm = 7,2.100/80 = 9
Nồng độ %: C% = 100S/(100 + S) = 7,2/(7,2 + 80) = 8,257%
Dạng 2: Tính lượng tinh thể ngậm nước cần thêm vào dung dịch
Cách làm: Dùng định luật bảo toàn khối lượng để tính:
- mdung dịch tạo thành = mtinh thể + mdung dịch ban đầu
- Khối lượng chất tan trong dung dịch tạo thành
m = mchất tan trong tinh thể + mchất tan trong dung dịch ban đầu.
Với những dạng toán tính lượng tinh thể ngậm nước này, đề bài thường cho sẵn loại tinh thể cần lấy và dung dịch cho sẵn có chứa cùng loại chất tan.
Bài 1: Tính lượng tinh thể CuSO4.5H2O cần lấy để pha chế 500 ml dung dịch CuSO4 8% (D = 1,1 g/ml).
Giải: Khối lượng CuSO4 có trong 500 ml CuSO4 8% là:
mCuSO4 = 500.1,1.8/100 = 44 gam ⇒ nCuSO4 = 0,275 mol
Vậy nCuSO4.5H2O = 0,275 mol
Khối lượng tinh thể CuSO4.5H2O là: m = 250.0,275 = 68,75 gam
Bài 2: Ở 25oC, có 175 gam dung dịch CuSO4 bão hòa. Đung nóng dung dịch lên 90oC, hỏi phải thêm vào dung dịch bao nhiêu gam CuSO4.5H2O để thu được dung dịch bão hòa ở nhiệt độ này. Biết độ tan của CuSO4 khan ở 25oC là 40 và ở 90oC là 80.
Giải:
Ở 25oC, mCuSO4 trong 175gam dung dịch là 40.175/140 = 50 gam
nH2O = 175 – 50 = 125 gam
Đặt a là khối lượng CuSO4.5H2O cần thêm vào:
Trong a gam CuSO4.5H2O có 160a/250 = 0,64a gam CuSO4 và 0,36 gam H2O
Vậy ở 90oC, sau khi thêm CuSO4.5H2O vào 175 gam dung dịch ta có:
mH2O = 125 + 0,36a
mCuSO4 = 50 + 0,64a
Ở 90oC: S = mCuSO4/mH2O = (50 + 0,64a)/(125 + 0,36a) = 80
⇒ a = 142 gam
Vận dụng: Để điều chế 560 gam dung dịch CuSO4 16% cần phải lấy bao nhiêu gam dung dịch CuSO4 8% và bao nhiêu gam tinh thể CuSO4.5H2O.
Dạng 3: Bài toán tính lượng chất tan tách ra hay thêm vào khi thay đổi một nhiệt độ dung dịch bão hòa cho sẵn.
Bài 1: Có 600 gam dung dịch NaCl bão hòa ở 90oC được làm lạnh xuống 0oC. Tính khối lượng kết tinh thu được biết độ tan của NaCl ở 90oC là 50, ở 0oC là 35.
Giải:
Ở 90oC, trong 600 gam dung dịch NaCl bão hòa có: 600.50/150 = 200 gam NaCl.
⇒ mH2O = 600 – 200 = 400 gam
Ở 0oC, trong 400 gam nước có: 400.35/135 = 140 gam
Vậy khối lượng muối NaCl tách ra khỏi dung dịch là 200 – 140 = 60 gam.
Bài 2: Lấy 1000 gam dung dịch Al2(SO4)3 bão hòa làm bay hơi 100 gam H2O. Phần dung dịch còn lại đưa về 10oC thấy có a gam Al2(SO4)3.18H2O kết tinh. Tính a. Biết độ tan của Al2(SO4)3 ở 10oC là 33,5.
Giải:
Xét trong 1000 gam dung dịch Al2(SO4)3 có 250,936 gam Al2(SO4)3 và 749,064 gam H2O
Trong a gam Al2(SO4)3.18H2O có 19a/37 gam Al2(SO4)3 và 18a/37 gam H2O.
Vậy sau khi kết tinh tách ra, dung dịch còn lại có chứa:
mct = 250,936 – 19a/37 (gam)
mH2O = 749,064 – 100 – 18a/37
Độ tan của Al2(SO4)3 ở 10oC là 33,5 nên ta có:
S = mct.100/mH2O = 95,565 gam
Vận dụng:
Bài 1: Giả thiết độ tan của CuSO4 ở 10oC và 80oC lần lượt là 17,4 và 55. Làm lạnh 1500 g dung dịch CuSO4 bão hòa ở 80oC xuống 10oC. Tính số gam CuSO4.5H2O tách ra khỏi dung dịch sau khi làm lạnh.
Bài 2: Xác định độ tan của Na2CO3 trong nước ở 18oC. Biết rằng ở nhiệt độ này, khi hòa tan hết 143 gam muối ngậm nước Na2CO3.10H2O trong 160 gam H2O thì thu được dung dịch bão hòa.

