- 13 Tháng chín 2017
- 2,335
- 4,740
- 584
- Nghệ An
- .
 [TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
[TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
 Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
Chắc suất Đại học top - Giữ chỗ ngay!!
ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
NGUYÊN LÝ THỨ NHẤT NHIỆT ĐỘNG HỌC
I. Khái niệm về hệ nhiệt động - trạng thái cân bằng - quá trình cân bằng – công và nhiệt của quá trình cân bằng
1, Hệ nhiệt động
Định nghĩa: Là một tập hợp các vật được xác định hoàn toàn bởi các thông số vĩ mô, độc lập với nhau.
Có 3 loại hệ nhiệt động là: hệ kín, hệ hở, và hệ cô lập.
2, Trạng thái cân bằng - quá trình cân bằng
Định nghĩa: Trạng thái cân bằng của hệ là trạng thái không biến đổi theo thời gian và tính bất biến đó không phụ thuộc vào các quá trình của ngoại vật.
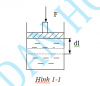
3, Công của áp lực trong quá trình cân bằng
Ngoại lực tác dụng lên pittông là F (hình 1-1).
Công của quá trình được tính bằng công thức:
[tex]A=\int \delta A=-\int_{v_1}^{v_2}pdv[/tex]
4, Nhiệt trong quá trình cân bằng, nhiệt dung
Nhiệt dung riêng c của một chất là một đại lượng vật lý về trị số bằng nhiệt lượng cần thiết truyền cho một đơn vị khối lượng chất ấy để nhiệt độ của nó tăng lên 10.
Gọi m là khối lượng của vật, dQ là nhiệt lượng truyền cho vật trong một quá trình cân bằng nào đó và dT là độ biến thiên nhiệt độ của vật trong quá trình đó thì:
[tex]δQ =n \int CdT[/tex]